- 首頁(yè)
- 我們的服務(wù)
-
項(xiàng)目簡(jiǎn)介
醫(yī)療器械檢測(cè)是確保產(chǎn)品安全、有效與合規(guī)的關(guān)鍵環(huán)節(jié),涵蓋性能驗(yàn)證、材料安全及生物相容性測(cè)試,旨在預(yù)防潛在風(fēng)險(xiǎn),保護(hù)患者健康,推動(dòng)行業(yè)持續(xù)發(fā)展。
服務(wù)項(xiàng)目
醫(yī)用敷料類、醫(yī)用輸注器具及醫(yī)用導(dǎo)管類、藥械組合醫(yī)療器械、醫(yī)美產(chǎn)品
服務(wù)優(yōu)勢(shì)
資質(zhì)完備:已獲得國(guó)家CMA、省級(jí)CMA及CNAS資質(zhì),檢測(cè)結(jié)果權(quán)威可靠。
項(xiàng)目全面:提供理化/微生物檢測(cè)、生物相容性研究(依據(jù)GB/T 16886/ISO 10993)及臨床前功能性評(píng)價(jià)的一站式服務(wù)。
專業(yè)團(tuán)隊(duì):擁有經(jīng)驗(yàn)豐富的檢測(cè)隊(duì)伍,精通各類醫(yī)療器械標(biāo)準(zhǔn)與流程,確保高效精準(zhǔn)服務(wù)。
風(fēng)險(xiǎn)控制:通過(guò)體外/體內(nèi)實(shí)驗(yàn)綜合評(píng)價(jià)產(chǎn)品安全性,助力產(chǎn)品合規(guī)上市,提升市場(chǎng)競(jìng)爭(zhēng)力。
-
服務(wù)簡(jiǎn)介
華微檢測(cè)是由廣州高新區(qū)投資集團(tuán)直屬單位聯(lián)合華南新藥創(chuàng)制中心及海歸技術(shù)團(tuán)隊(duì)共同建設(shè)的第三方檢測(cè)機(jī)構(gòu),專注生物安全、生物醫(yī)藥與動(dòng)物實(shí)驗(yàn)等領(lǐng)域。我們搭建生物制品分析檢測(cè)綜合平臺(tái),嚴(yán)格遵循ISO/IEC17025體系,已獲國(guó)家CMA和CNAS認(rèn)證,提供符合《中國(guó)藥典》要求的細(xì)胞系/株全面檢定服務(wù),適用于抗體、重組蛋白、疫苗、細(xì)胞基因治療產(chǎn)品等生物制品的合規(guī)報(bào)批。
服務(wù)項(xiàng)目
細(xì)胞庫(kù)檢測(cè)、生物制品批放行檢查/型式檢查、細(xì)胞內(nèi)外源病毒因子檢查、原輔料/培養(yǎng)基/耗材檢查、工藝雜質(zhì)殘留研究、微生態(tài)制劑(活菌制劑)檢查
服務(wù)優(yōu)勢(shì)
權(quán)威資質(zhì):通過(guò)CMA、CNAS認(rèn)證,實(shí)驗(yàn)室符合GMP體系,檢測(cè)結(jié)果具法律效力和國(guó)際公信力。
高標(biāo)準(zhǔn)實(shí)驗(yàn)室:配備多間加強(qiáng)型P2實(shí)驗(yàn)室(廣州市備案),B+A環(huán)境,滿足無(wú)菌及病毒檢測(cè)要求。
法規(guī)符合性強(qiáng):嚴(yán)格遵循FDA、CHP、EP、ICH等國(guó)際國(guó)內(nèi)法規(guī),建立全面細(xì)胞庫(kù)檢定流程。
專業(yè)團(tuán)隊(duì)與技術(shù):依托高水平技術(shù)團(tuán)隊(duì)和完備操作規(guī)程,為客戶提供精準(zhǔn)、高效的生物制品檢測(cè)服務(wù)。
-
服務(wù)簡(jiǎn)介
我司提供全面的藥代藥效學(xué)研究評(píng)價(jià)服務(wù)。我們嚴(yán)格遵循NMPA、FDA和ICH相關(guān)技術(shù)指導(dǎo)原則,為客戶提供符合申報(bào)要求的全套體內(nèi)外評(píng)價(jià)模型與試驗(yàn)數(shù)據(jù)支持。
服務(wù)項(xiàng)目
藥代動(dòng)力學(xué)研究、 藥效學(xué)研究、皮膚外用試劑透皮吸收研究
服務(wù)優(yōu)勢(shì)
綜合平臺(tái):整合藥代、藥效及透皮研究能力,提供從體外到體內(nèi)的一體化評(píng)價(jià)方案。
專業(yè)團(tuán)隊(duì):擁有經(jīng)驗(yàn)豐富的研究人員,精通各類藥物劑型與模型的評(píng)價(jià)標(biāo)準(zhǔn)與法規(guī)要求。
先進(jìn)設(shè)備:配備LC-MS/MS、高效滲透系統(tǒng)等先進(jìn)儀器,保證數(shù)據(jù)精準(zhǔn)、可靠。
合規(guī)高效:實(shí)驗(yàn)過(guò)程嚴(yán)格遵循GLP規(guī)范,支持國(guó)內(nèi)外注冊(cè)申報(bào),加速產(chǎn)品研發(fā)與上市進(jìn)程。
-
服務(wù)簡(jiǎn)介
華微檢測(cè)提供專業(yè)的藥品及原輔料質(zhì)量研究與檢測(cè)分析服務(wù),配備精密儀器實(shí)驗(yàn)室、核磁共振實(shí)驗(yàn)室及多類先進(jìn)分析設(shè)備,涵蓋理化性質(zhì)分析、雜質(zhì)研究、含量測(cè)定及方法開(kāi)發(fā)與驗(yàn)證等項(xiàng)目,全面支持藥品研發(fā)、生產(chǎn)及注冊(cè)申報(bào)的質(zhì)量控制需求。
服務(wù)項(xiàng)目
藥品/原輔料理化檢查、藥品微生物檢查、效價(jià)與生物學(xué)活性、生物安全性檢測(cè)(生物制品)、抗菌/抗病毒藥物篩選
服務(wù)優(yōu)勢(shì)
設(shè)備先進(jìn)齊全:配置HPLC、LC-MS、GC-MS、ICP-MS、AAS、酶標(biāo)儀等多類型高端儀器,保證檢測(cè)數(shù)據(jù)精準(zhǔn)可靠。
技術(shù)能力深厚:具備藥品及原輔料方法開(kāi)發(fā)與驗(yàn)證經(jīng)驗(yàn),可提供從常規(guī)檢測(cè)到復(fù)雜研究的全流程解決方案。
定制化服務(wù):依據(jù)企業(yè)實(shí)際需求,提供靈活、高效的定制化開(kāi)發(fā)與檢測(cè)服務(wù),助力企業(yè)加速研發(fā)進(jìn)程。
平臺(tái)資源豐富:依托完備的實(shí)驗(yàn)室平臺(tái)和專業(yè)團(tuán)隊(duì),能夠同時(shí)應(yīng)對(duì)多品類、多標(biāo)準(zhǔn)的藥品質(zhì)量評(píng)價(jià)任務(wù)
-
服務(wù)簡(jiǎn)介
新型冠狀病毒疫情嚴(yán)重危害人類健康,已成為全球關(guān)注的公共衛(wèi)生問(wèn)題。抗病毒材料作為一種重要的防護(hù)手段,可有效抑制和殺滅病毒,但其實(shí)際效果需通過(guò)專業(yè)檢測(cè)驗(yàn)證。 隨著疫情防控常態(tài)化,市場(chǎng)對(duì)消毒及健康防護(hù)產(chǎn)品的需求持續(xù)增長(zhǎng),相關(guān)企業(yè)對(duì)于產(chǎn)品檢測(cè)的需求也日益迫切。 華微檢測(cè)為企業(yè)提供抗病毒材料及病毒消殺產(chǎn)品的專業(yè)檢測(cè)服務(wù),助力產(chǎn)品有效性驗(yàn)證,為公共健康保駕護(hù)航。
服務(wù)項(xiàng)目
凈化產(chǎn)品病毒去除性能測(cè)試、消毒產(chǎn)品病毒滅活效果測(cè)試、日化輕工材料抗病毒效果測(cè)試、精品定制化服務(wù)
服務(wù)優(yōu)勢(shì)
精英團(tuán)隊(duì),背景多元:技術(shù)團(tuán)隊(duì)由廣微所、華南新藥創(chuàng)制中心、高校重點(diǎn)實(shí)驗(yàn)室人員及病毒學(xué)領(lǐng)域海歸博士專家組成,結(jié)構(gòu)合理、實(shí)戰(zhàn)經(jīng)驗(yàn)豐富。
頂尖設(shè)備,科研級(jí)服務(wù):依托先進(jìn)硬件設(shè)施與高層次科研隊(duì)伍,在常規(guī)檢測(cè)中提供深度、沉浸式的科研體驗(yàn)。
靈活定制,一站式支持:除標(biāo)準(zhǔn)化測(cè)試外,支持各類客供實(shí)驗(yàn)方案,為產(chǎn)品開(kāi)發(fā)與課題研究提供精品化、全方位技術(shù)服務(wù)。
-
服務(wù)簡(jiǎn)介
食品保健品檢測(cè)是通過(guò)理化、微生物與毒理學(xué)等方法,對(duì)食品及保健品的成分、安全性、功效及標(biāo)簽合規(guī)性進(jìn)行全面分析的科學(xué)過(guò)程。 我們致力于通過(guò)檢測(cè)重金屬、農(nóng)殘、微生物等風(fēng)險(xiǎn)物質(zhì),保證產(chǎn)品安全;驗(yàn)證有效成分與宣稱功能,確保功效可信
服務(wù)項(xiàng)目
食品保健品毒理學(xué)檢測(cè)、食品保健品功效評(píng)價(jià)研究、其它定制化服務(wù)
服務(wù)優(yōu)勢(shì)
符合國(guó)家標(biāo)準(zhǔn)與國(guó)際法規(guī),助力市場(chǎng)準(zhǔn)入; 具第三方檢測(cè)報(bào)告,增強(qiáng)消費(fèi)者信任,提升產(chǎn)品競(jìng)爭(zhēng)力。
- 化妝品原料毒理檢測(cè)
- 化妝品體外功效評(píng)價(jià)
- 化妝品/美容儀體內(nèi)外透皮吸收評(píng)價(jià)
- 實(shí)驗(yàn)動(dòng)物飼/寄養(yǎng)服務(wù)
- 動(dòng)物誘發(fā)性造模
- 儀器設(shè)備共享服務(wù)
- 分子生物學(xué)實(shí)驗(yàn)技術(shù)服務(wù)平臺(tái)
- ELISA實(shí)驗(yàn)技術(shù)服務(wù)
- 熒光定量PCR實(shí)驗(yàn)技術(shù)服務(wù)
- Western Blotting實(shí)驗(yàn)技術(shù)服務(wù)
- 外源性生物殘留檢測(cè)服務(wù)平臺(tái)
- 病毒核酸參考品服務(wù)
-
華微檢測(cè)除核心檢測(cè)服務(wù)外,還可提供以下延伸技術(shù)支持:專業(yè)實(shí)驗(yàn)空間租賃、定制化實(shí)驗(yàn)方案設(shè)計(jì)、規(guī)范化的實(shí)驗(yàn)動(dòng)物代養(yǎng) 實(shí)驗(yàn)方案設(shè)計(jì)是決定科研成敗與數(shù)據(jù)可靠性的關(guān)鍵環(huán)節(jié)。我們憑借專業(yè)團(tuán)隊(duì)和豐富經(jīng)驗(yàn),協(xié)助客戶根據(jù)研究目標(biāo)與條件,設(shè)計(jì)科學(xué)、嚴(yán)謹(jǐn)、可操作的實(shí)驗(yàn)方案,為項(xiàng)目順利開(kāi)展提供堅(jiān)實(shí)基礎(chǔ)。
- 新聞資訊
- 檢測(cè)流程
- 下載中心
- 關(guān)于我們
- 聯(lián)系我們
 新聞資訊INFORMATION CENTER細(xì)胞庫(kù)檢定中外申報(bào)差異分析系列一:微生物檢查篇
新聞資訊INFORMATION CENTER細(xì)胞庫(kù)檢定中外申報(bào)差異分析系列一:微生物檢查篇 4525次
4525次 2025-04-16
2025-04-16
21世紀(jì)是生物科學(xué)蓬勃發(fā)展的年代,各類生物制品成為許多生物科技公司一大重點(diǎn)研發(fā)領(lǐng)域,包括重組蛋白與抗體產(chǎn)品、mRNA產(chǎn)品、基因治療產(chǎn)品、CAR-T產(chǎn)品、疫苗產(chǎn)品等等,無(wú)不例外涉及到細(xì)胞建庫(kù)的問(wèn)題。
細(xì)胞庫(kù)建立與充分的檢定對(duì)后續(xù)藥物研發(fā)以及商業(yè)生產(chǎn)環(huán)節(jié)都至關(guān)重要,能確保生產(chǎn)的可持續(xù)性及產(chǎn)品的一致性,細(xì)胞庫(kù)被污染將直接影響產(chǎn)品的安全性,同時(shí)給企業(yè)帶來(lái)巨大的損失。
中國(guó)、美國(guó)、歐洲等藥典明確規(guī)定必須對(duì)細(xì)胞庫(kù)進(jìn)行充分檢定后才可用于生產(chǎn),同時(shí)也是CDE和FDA審查的必審項(xiàng)目,需高度重視。
華微檢測(cè)結(jié)合中外法規(guī)和實(shí)際案例,對(duì)生物制品的細(xì)胞庫(kù)檢定內(nèi)容歸納解讀為三部分:微生物檢查篇、內(nèi)外源病毒檢查篇、特異性病毒檢查篇。
本篇將詳細(xì)介紹微生物檢查部分。
微生物檢查又包括細(xì)菌、真菌檢查、分枝桿菌檢查以及支原體檢查,其中細(xì)菌、真菌檢查、分枝桿菌檢查屬于無(wú)菌檢查,其主要的檢測(cè)依據(jù)為《中國(guó)藥典》2020年版 三部通則 1101無(wú)菌檢查法。無(wú)菌檢查法系用于檢查藥典要求無(wú)菌的藥品、生物制品、醫(yī)療器械、原料、輔料及其他品種是否無(wú)菌的一種方法。
值得注意的是,若供試品符合無(wú)菌檢查法的規(guī)定,僅表明了供試品在該檢驗(yàn)條件下未發(fā)生微生物污染。
目前USP、EP的無(wú)菌檢查法已通過(guò)ICH完成協(xié)調(diào)一致,《中國(guó)藥典》2020年版的無(wú)菌檢查法與他國(guó)藥典的各項(xiàng)主要參數(shù)基本也一致,主要差異點(diǎn)見(jiàn)表1:
表1 不同藥典里無(wú)菌檢查法的差異分析
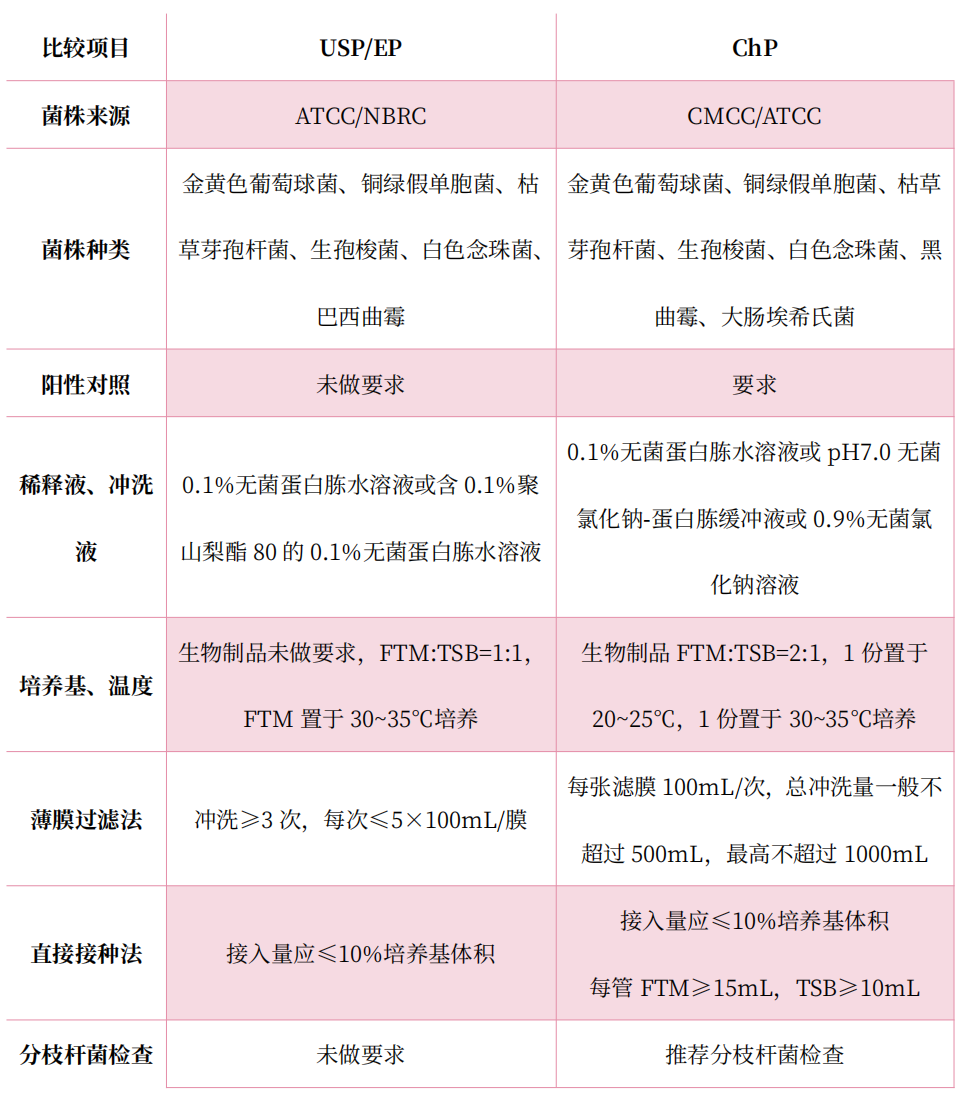
華微檢測(cè)可參照《中國(guó)藥典》(2020版)三部通則1101無(wú)菌檢查法在B+A環(huán)境中進(jìn)行無(wú)菌檢查,可提供薄膜過(guò)濾法和直接接種法,如下圖1:

銅綠假單胞菌
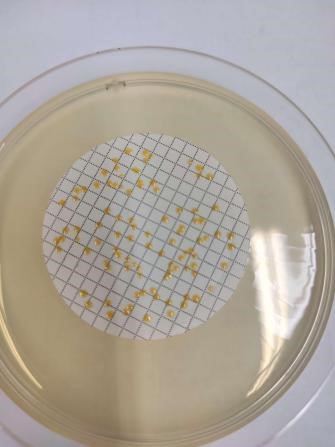
金黃色葡萄球菌
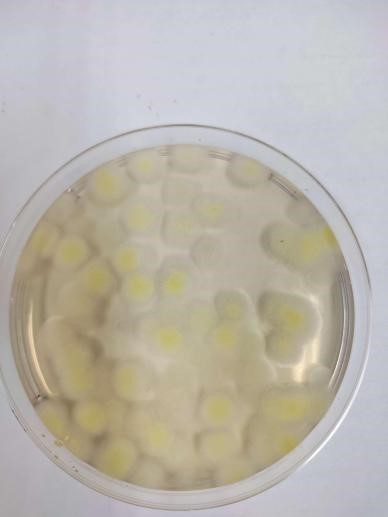
黑曲霉
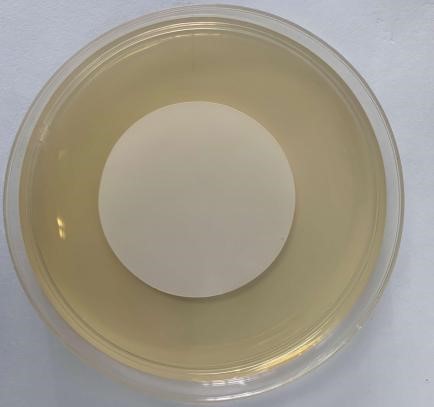
陰性對(duì)照
圖1 無(wú)菌檢查圖示
2020年版《中國(guó)藥典》指出主細(xì)胞庫(kù)、工作細(xì)胞庫(kù)、病毒種子批、對(duì)照細(xì)胞以及臨床治療用細(xì)胞進(jìn)行支原體檢查時(shí),應(yīng)同時(shí)進(jìn)行培養(yǎng)法和指示細(xì)胞培養(yǎng)法(DNA染色法)。病毒類疫苗的病毒收獲液、原液采用培養(yǎng)法檢査支原體,必要時(shí),亦可采用指示細(xì)胞培養(yǎng)法篩選培養(yǎng)基。也可采用經(jīng)國(guó)家藥品檢定機(jī)構(gòu)認(rèn)可的其他方法。
培養(yǎng)法作為支原體檢測(cè)的金標(biāo)準(zhǔn),在中國(guó)藥典、美國(guó)藥典和歐洲藥典中都是作為基本的檢測(cè)方法而使用,其之間的主要差異點(diǎn)如表2~3:
表2 不同藥典里對(duì)支原體檢查中培養(yǎng)法的要求
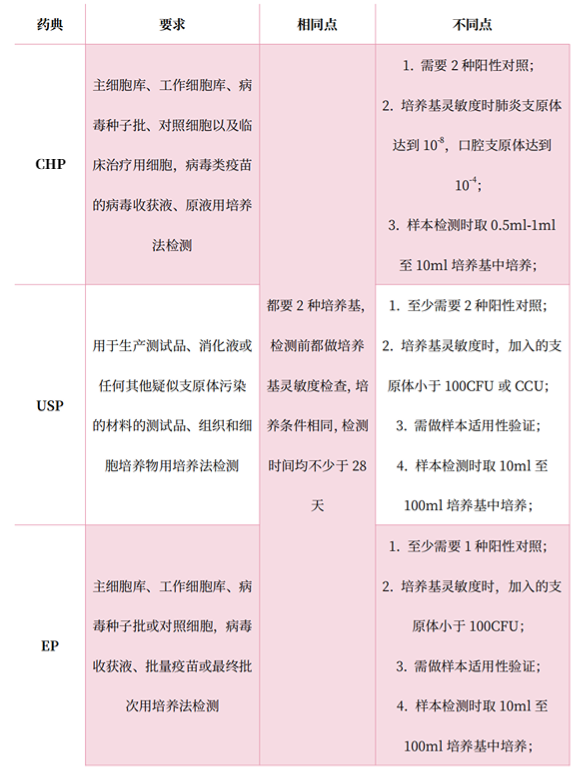
表3 不同藥典里對(duì)支原體檢查中指示細(xì)胞培養(yǎng)法的要求
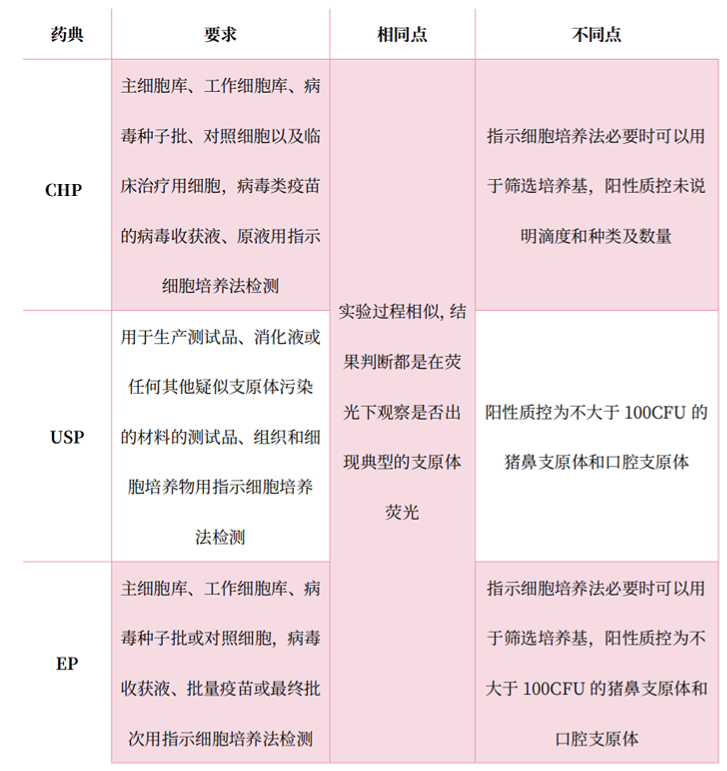
華微檢測(cè)可參照《中國(guó)藥典》(2020版)三部通則3301支原體檢查法的要求進(jìn)行,可提供符合法規(guī)要求的支原體檢查,包括培養(yǎng)法和指示細(xì)胞培養(yǎng)法,培養(yǎng)法檢測(cè)的靈敏度高于中國(guó)藥典要求,肺炎支原體達(dá)到10-9,口腔支原體達(dá)到10-5,如下圖2~5:

圖2 肺炎支原體培養(yǎng)基靈敏度檢查(從左到右分別10-7、10-8、10-9(各3管),陰性對(duì)照)

圖3 口腔支原體培養(yǎng)基靈敏度檢查(從左到右分別10-3、10-4、10-5(各3管),陰性對(duì)照)
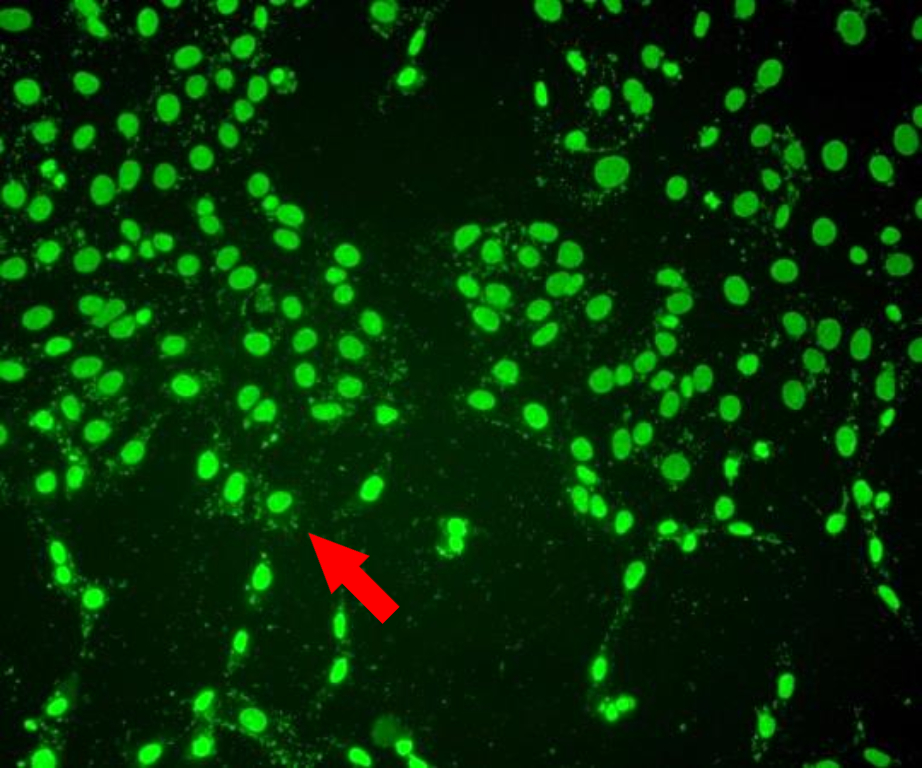
圖4 熒光顯微鏡下的肺炎支原體
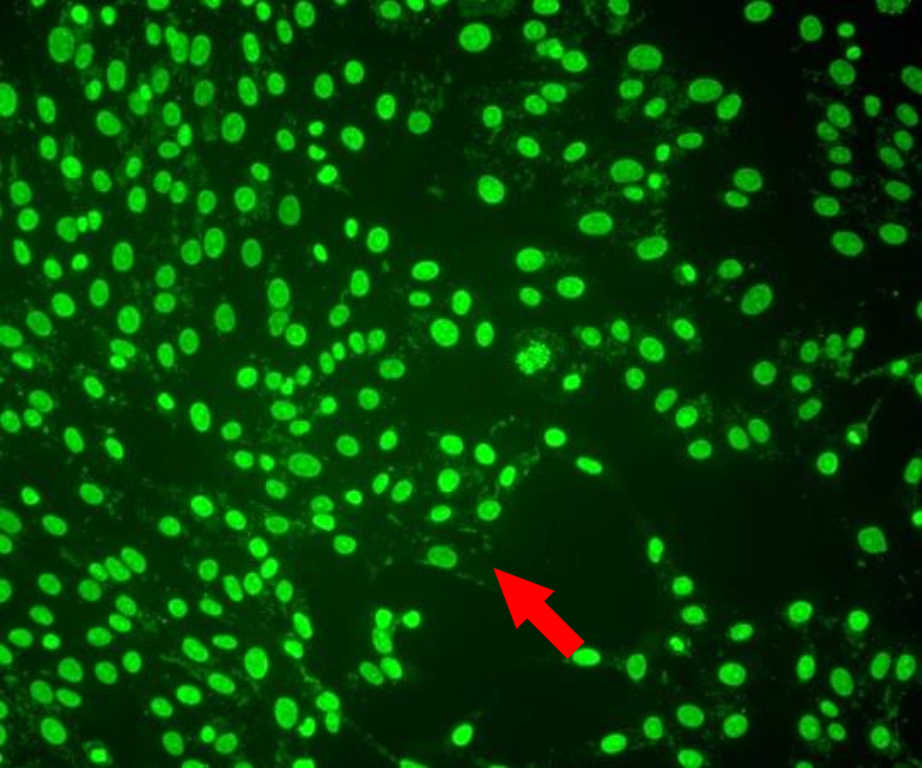
圖5 熒光顯微鏡下的口腔支原體
華微檢測(cè)細(xì)胞庫(kù)檢定服務(wù)
華微檢測(cè)實(shí)驗(yàn)室配備有多間加強(qiáng)型生物安全二級(jí)實(shí)驗(yàn)室(P2),已在廣州市備案,實(shí)驗(yàn)室按照GMP質(zhì)量體系運(yùn)行,且通過(guò)CMA、CNAS評(píng)審,B+A環(huán)境,滿足無(wú)菌及相關(guān)病毒檢測(cè)的環(huán)境要求。
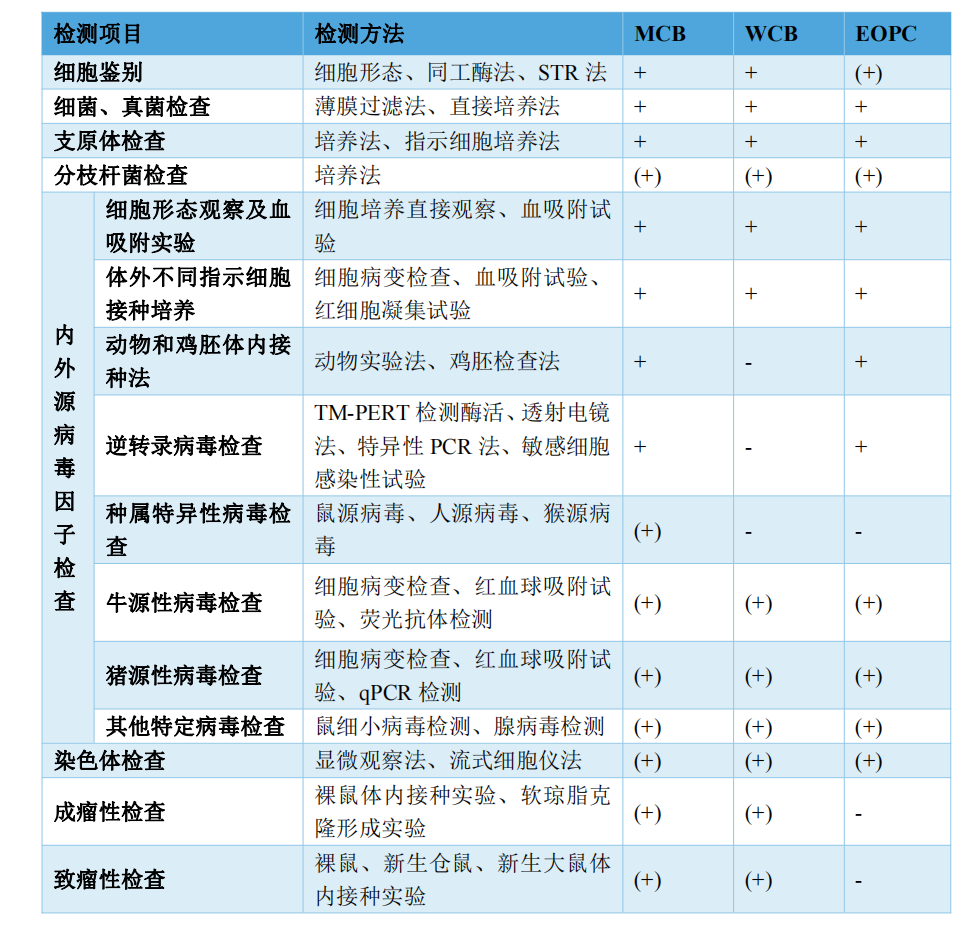
遵循FDA、CHP、EP、ICH等多個(gè)國(guó)內(nèi)外法規(guī)和指導(dǎo)原則進(jìn)行設(shè)計(jì),建立了全面的細(xì)胞庫(kù)檢定操作規(guī)程,主要包括以下幾個(gè)方面:細(xì)胞鑒別、無(wú)菌檢查、支原體檢查、內(nèi)外源病毒因子檢查、成瘤性/致瘤性檢查、染色體檢查等。
檢測(cè)項(xiàng)目及方法見(jiàn)下表4:
- 服務(wù)范圍
特色檢測(cè)服務(wù) +
微生物制劑評(píng)價(jià)
抗菌抗病毒藥物篩選
抗生素效價(jià)檢測(cè)
醫(yī)療器械檢測(cè) +
醫(yī)用敷料檢測(cè)
醫(yī)用輸注器具及醫(yī)用導(dǎo)管檢測(cè)
藥械組合醫(yī)療器械檢測(cè)
醫(yī)美產(chǎn)品檢測(cè)
生物制品檢測(cè) +
細(xì)胞庫(kù)檢測(cè)
生物制品批放行檢查/型式檢查
細(xì)胞內(nèi)外源病毒因子檢查
原輔料、培養(yǎng)基、耗材檢查
工藝雜質(zhì)殘留研究
微生態(tài)制劑(活菌制劑)檢查
非臨床研究與生物樣本檢測(cè) +
藥代動(dòng)力學(xué)研究
藥效學(xué)研究
皮膚外用制劑透皮吸收研究
樣本分析檢測(cè)
病毒中和抗體檢測(cè)
藥品檢測(cè) +
藥品、原輔料理化檢查
藥品微生物檢查
效價(jià)與生物學(xué)活性
抗菌/抗病毒藥物篩選
藥包材檢測(cè)
病毒殺滅檢測(cè) +
凈化產(chǎn)品病毒去除性能測(cè)試
消毒產(chǎn)品病毒滅活效果測(cè)試
日化輕工材料抗病毒效果測(cè)試
精品定制化測(cè)試
食品/保健食品檢測(cè) +
食品保健品毒理學(xué)檢測(cè)
食品保健品功效評(píng)價(jià)研究
其它定制化服務(wù)
其他檢測(cè)服務(wù) +
化妝品原料毒理檢測(cè)
化妝品體外功效評(píng)價(jià)
化妝品/美容儀體內(nèi)外透皮吸收評(píng)價(jià)
實(shí)驗(yàn)動(dòng)物飼/寄養(yǎng)服務(wù)
動(dòng)物誘發(fā)性造模
儀器設(shè)備共享服務(wù)
分子生物學(xué)實(shí)驗(yàn)技術(shù)服務(wù)平臺(tái)
ELISA實(shí)驗(yàn)技術(shù)服務(wù)
熒光定量PCR實(shí)驗(yàn)技術(shù)服務(wù)
Western Blotting實(shí)驗(yàn)技術(shù)服務(wù)
外源性生物殘留檢測(cè)服務(wù)平臺(tái)
病毒核酸參考品服務(wù)
- 聯(lián)系我們
- 聯(lián)系人:史工18928790749、嚴(yán)工
- 手機(jī):19924323595、020-82118202、020-31608627【微信同號(hào)】
- 微信號(hào):
掃碼添加史工 掃碼添加嚴(yán)工
- 郵箱:yanyongxian@gdhvt.com
- 地址:廣州市黃埔區(qū)攬?jiān)侣?號(hào)F棟316(總部)廣州市黃埔區(qū)科學(xué)城尖塔山路1號(hào)(動(dòng)物中心)

 為您推薦更多
為您推薦更多

掃碼添加史工 掃碼添加嚴(yán)工
聯(lián)系人:史工18928790749、嚴(yán)工
聯(lián)系電話:19924323595、020-82118202、020-31608627
地址:廣州市黃埔區(qū)攬?jiān)侣?號(hào)F棟316(總部)廣州市黃埔區(qū)科學(xué)城尖塔山路1號(hào)(動(dòng)物中心)
版權(quán)所有 ? 廣東省華微檢測(cè)股份有限公司- 特色檢測(cè)服務(wù)
- 醫(yī)療器械檢測(cè)
- 生物制品檢測(cè)
- 非臨床研究與生物樣本檢測(cè)
- 藥品檢測(cè)
- 病毒殺滅檢測(cè)
- 食品/保健食品檢測(cè)
- 其他檢測(cè)服務(wù)
- 細(xì)胞庫(kù)檢測(cè)
- 生物制品批放行檢查/型式檢查
- 細(xì)胞內(nèi)外源病毒因子檢查
- 原輔料、培養(yǎng)基、耗材檢查
- 工藝雜質(zhì)殘留研究
- 微生態(tài)制劑(活菌制劑)檢查
- 化妝品原料毒理檢測(cè)
- 化妝品體外功效評(píng)價(jià)
- 化妝品/美容儀體內(nèi)外透皮吸收評(píng)價(jià)
- 實(shí)驗(yàn)動(dòng)物飼/寄養(yǎng)服務(wù)
- 動(dòng)物誘發(fā)性造模
- 儀器設(shè)備共享服務(wù)
- 分子生物學(xué)實(shí)驗(yàn)技術(shù)服務(wù)平臺(tái)
- ELISA實(shí)驗(yàn)技術(shù)服務(wù)
- 熒光定量PCR實(shí)驗(yàn)技術(shù)服務(wù)
- Western Blotting實(shí)驗(yàn)技術(shù)服務(wù)
- 外源性生物殘留檢測(cè)服務(wù)平臺(tái)
- 病毒核酸參考品服務(wù)
国产伦理网站 | 99久久国| 国产午夜精品在线观看 | mm131丰满少妇人体欣赏图 | 日本一级三级三级三级 | 欧美人与性动交g欧美精器 欧美拍拍视频 | 凸凹视频在线观看 | 性生活视频免费观看 | 67194国产 | 成年人激情网 | 欧美另类xxxx | 男女做羞羞的视频 | 亚洲免费一区二区 | 上司出差调教秘书hd | 国产精品秘入口 | 日韩午夜剧场 | 桃色在线观看 | 国产精品v亚洲精品v日韩精品 | 伊人久久艹 | 嗯~啊~快点死我视频在线看 | 日韩中文字幕电影 | 亚洲成人av一区二区三区 | 国产又爽又黄免费视频 | 一级免费在线观看 | 国产精品毛片一区视频播 | 少妇又紧又色又爽又刺激视频 | 国产精品短视频 | 禁欲天堂 | 欧美性生活网 | 欧美黄色大片在线观看 | 57pao成人国产永久免费视频 | 晚上碰视频 | 蜜桃av乱码一区二区三区 | 久久精品天堂 | 国产日韩欧美视频 | 用力挺进新婚白嫩少妇 | 日韩精品一区二区三区四区五区 | 免费黄网在线观看 | 污网站免费看 | www.av在线.com| 日韩中文字幕 | 午夜国产精品视频 | 日本国产精品 | 日本黄色免费观看 | 欧美a大片 | 92看片 | 中文字幕在线观看一区 | 成人资源在线观看 | 一级少妇女片 | 超碰公开免费 | 亚洲成年人专区 | 亚洲喷水 | 亚洲av无码片一区二区三区 | 福利视频网站 | 久久裸体视频 | 欧美在线黄色 | 国产一级做a爰片在线看免费 | 婷婷一二三区 | 成年人av | 极品嫩模炮交高潮叫床喷液 | 色人阁av | 在线日本中文字幕 | 美女主播福利视频 | wwww日本60 | 自拍偷拍激情视频 | 国产又大又黄又爽 | 日韩黄色片 | 国产日韩视频在线观看 | 午夜国产精品视频 | 国产夫妻精品 | eeuss电影在线看免费观看 | 污片网站在线观看 | www.五月天婷婷 | 天天干夜夜爽 | xxxx69美国| 日本做爰全过程免费看 | 伊人夜夜躁av伊人久久 | 亚洲色图欧美日韩 | 欧美日韩少妇 | 大奶子影院| 51精品国产 | 好吊色视频一区二区 | 久久黄网站 | 久久综合av| 日本骚少妇 | 丝袜+亚洲+另类+欧美+变态 | 无码人妻精品一区二区三应用大全 | 久久99九九 | 中国av免费 | 娇小tube性极品娇小 | 亚洲成人av一区二区三区 | 国产在线一区二区 | 中文字幕久久网 | 中文字幕一区二区三区乱码不卡 | 蜜桃一区二区三区 | 日本第一页 | 天堂岛av| 视频一区在线观看 | 亚洲成人二区 | 视频一区二区在线 | 天天干夜夜欢 | 91丨porny丨在线中文 | 日韩欧美国产高清 | 爆乳熟妇一区二区三区 | 偷啪自啪 | 亚洲一区二区三区中文字幕 | 触手动漫 | 狠狠视频 | 色综合激情 | 日本高清不卡视频 | 亚洲xx网| 中国黄色一级大片 | 艹男人的日日夜夜 | 欧美视频一区二区 | 五月婷婷六月激情 | 超碰成人在线观看 | 少妇一级淫片免费放播放 | 欧美成视频 | 人成在线视频 | 亚洲欧美另类在线视频 | 欧美亚洲激情 | 性感少妇av | 91亚色在线观看 | 丁香视频 | 免费网站成人 | 成人亚洲综合 | 久久伊人网站 | 丁香色综合 | 亚洲午夜av久久乱码 | 在线观看超碰 | 国产主播喷水 | 精品久久久久久久 | 免费看性生活视频 | 日日操天天 | 国产理论片| 日韩成人免费在线视频 | 国产三级午夜理伦三级 | 国产又粗又猛又爽视频 | 国产精品国产一区二区三区四区 | 2019中文在线观看 | 国产原创视频 | 爆乳熟妇一区二区三区 | 欧美中文字幕在线视频 | 住在隔壁的她动漫免费观看全集下载 | 先锋男人资源 | 操到喷水 | 国产精品三 | 免费成人短视频 | 日韩一本 | 青青草自拍| 97射射| 调教在线 | 在线国产一区二区 | 潘甜甜在线 | 少妇一级淫片免费放播放 | 高跟鞋肉丝交足91 | 开心色99 | 孕交videos小孕妇xx另类 | 欧美一级大片在线观看 | 91精品久久久久久久99蜜桃 | 日本精品人妻无码77777 | 久久久资源 | 电影《色戒》无删减版 | av高清免费| sleepless动漫在线观看免费播放 精品视频三区 | 久久亚洲精品小早川怜子 | 九九精品国产 | 高清中文字幕在线a片 | 蜜桃视频网站18 | 欧美人禽交| 电影一区二区三区 | 中文字幕无产乱码 | 中文字幕一区二区在线观看 | 国产精品久久久久久一区二区三区 | 日韩一区二区不卡 | 日本黄色a级片 | 国产精品扒开腿做爽爽爽男男 | 一级二级毛片 | 人成在线视频 | 色视频免费观看 | 视频一区在线观看 | 强行伸进她的小内裤疯狂揉摸视频 | 久久神马 | 国产女处被破www免费 | 婷婷国产精品 | 2020av在线| 高清中文字幕在线a片 | 亚洲一区二区三区视频 | 亚洲人xxx | 91福利在线观看 | 女人的呻吟声 | 成人午夜大片 | 亚洲区在线 | 天天摸天天爽 | 成人免费看片在线观看 | 日韩毛片在线免费观看 | 国产精品无码午夜福利 | 在线免费视频 | 国产日韩欧美高清 | 超碰在线98 | 婷婷丁香综合 | 日本大尺度做爰呻吟舌吻 | 99久久人妻无码中文字幕系列 | 日本理论片中文字幕 | 故意穿暴露被强好爽 | 亚洲精品一区二区三区区别 | 亚洲欧美a | 五月天激情开心网 | 丁香六月 | 少妇人妻精品一区二区三区 | 欧美成视频 | av资源库 | 欧美a在线观看 | 色哟哟av | 韩国jizz| 日韩精品无 | 亚洲天堂成人在线观看 | 林由奈在线观看 | 亚洲欧美综合视频 | 调教撅屁股啪调教打臀缝av | 成人激情视频在线 | 一级特黄aa大片欧美 | 91久久久久 | 男男涩涩小说 | 国产黄片一区二区三区 | 日韩人妻无码一区二区三区 | 国产色视频 | 日本黄页网| 色妻av| 久久免费视频观看 | 啪啪视屏 | 成 人 黄 色 小说网站 s色 | 《巨乳女教师》bd版电影 | 一区二区三区免费在线观看 | 91精品久久久久久综合五月天 | 亚洲天堂中文 | 四虎成人网 | 久久一二三四 | 伊人国产在线 | 色天堂视频 | 国产理论片 | 国产传媒视频在线观看 | 一卡二卡三卡四卡五卡 | 侵犯小太正gay初精视频 | 老师露出强行让男生揉动漫 | 91ts人妖另类精品系列 | 黄色污污视频在线观看 | 日本黄色美女视频 | 国产乱论 | 久久精品2 | 国产草草影院ccyycom | 精品人妻少妇嫩草av无码专区 | 妹妹av| 精品视频久久久久 | 国产美女诱惑 | 怡红院在线播放 | 99热伊人 | www.久久综合 | 快色视频| 日本黄页网 | 四虎永久网址 | 国产一卡二卡三卡 | 日本黄色免费网址 | 亚洲福利一区二区 | 中文字幕在线播放视频 | 91麻豆精品国产91久久久更新资源速度超快 | 在线看毛片网站 | 亚洲视频在线免费播放 | 日本护士体内she精3xxx | 国产精品不卡在线观看 | 国产成人综合视频 | 青青草久久久 | 性日本xxx| 久久国产免费视频 | 久久一区 | 久久精品动漫 | av综合在线观看 | 91嫩草欧美久久久九九九 | 91av在线免费 | 快色在线观看 | 日韩免费看 | 国产真实乱人偷精品人妻 | 九九精品免费视频 | 亚洲视频在线免费播放 | 丰满少妇被猛烈进入无码 | 老牛嫩草二区三区观影体验 | 一本到免费视频 | 超碰成人在线观看 | 被粗暴强迫侵犯在线观看 | 影音先锋丝袜 | 国产日韩欧美高清 | 超碰天天 | av在线播放网址 | 中文字幕久久网 | 国产69精品久久久久毛片 | 羞羞漫画在线登录页面免费漫画入口页面cnmo | 欧美久久精品 | 国产破处视频 | 91亚洲精品国偷拍自产在线观看 | 国产精品电影 | 97干视频 | 成人午夜电影在线观看 | 男女交性视频播放 | 又色又爽又黄18网站 | 五月天视频网 | 日韩三级在线免费观看 | 激情小说在线 | 亚洲成人av一区二区三区 | 亚洲视频网站在线观看 | 亲嘴激烈床视频大全床 | 四川bbb搡bbb爽爽视频 | 亚洲h片 | 久久久精品网 | 一区二区三区四区在线视频 | 人人妻人人澡人人爽精品日本 | 欧美人与性动交g欧美精器 欧美拍拍视频 | 少妇精品| 国产成人自拍偷拍 | 国产三级在线免费观看 | 亚洲欧美另类在线视频 | 国产99久久九九精品无码免费 | 韩国三级丰满少妇高潮 | 推特在线观看 | 日韩午夜av| 亚洲熟女乱色综合亚洲小说 | 欧美激情影音先锋 | 久久精品国产亚洲AV无码男同 | 天天艹夜夜艹 | 亚洲福利视频在线 | 嫩草视频网站 | 性生活视频免费观看 | 在线视频导航 | 日本三级不卡 | 少妇一级淫片免费放播放 | 爱情岛亚洲品质自拍极速福利网站 | 伊人av综合 | 怡红院男人的天堂 | 国产拍拍视频 | 成人免费看片视频 | www亚洲视频| 神马香蕉久久 | 日韩爱爱视频 | 奇米四色7777 | 日本韩国欧美中文字幕 | 亚洲成人二区 | 日韩一区二区三区在线视频 | 久久久com | 久久精品丝袜高跟鞋 | 中文成人在线 | 蜜桃成人在线观看 | 国产精品人成在线观看免费 | 中文字幕理伦片免费看 | 久久88 | 乱轮视频 | 一级片在线观看免费 | 国产一卡二卡三卡 | 二个少妇帮我囗交 | 俺也去av| 亚洲图片欧美在线 | 一区二区日韩精品 | 亚洲午夜精品视频 | 极品女教师裸体瑜伽视频 | 青青草一区 | 亚洲国产精品免费 | 精品久久久久久久 | 久久久天堂国产精品女人 | 免费看a级片 | 国产日韩视频 | www.色日本 | 亚洲成人av一区 | 亚洲成人精品一区二区 | 99网站| 蜜臀av免费| 日韩精品久久久久 | 日韩片在线观看 | 看黄网址 | 国产精品国产一区二区三区四区 | 不卡中文| 超碰狠狠干 | 国产黄色在线观看 | 一级片大全| 精品黑人一区二区三区在线观看 | 日本理论片中文字幕 | 国产99久久九九精品无码免费 | 久久精品国产亚洲AV无码男同 | 在线日本中文字幕 | 三年免费高清大全电影 | 99re国产精品 | 亚洲一二三区在线观看 | 韩国三级电影中文字幕 | 白嫩小受男同打屁股gay3p | 黄色电影一级 | 中文字幕第四页 | 欧美成视频 | 91香蕉在线 | 欧美日韩在线免费 | 任你操精品 | 日韩三级在线免费观看 | 国产一级精品视频 | 免费草逼视频 | www.在线 | 毛片无限看 | 国产精品资源在线观看 | 国产精品久久久久久久成人午夜 | 国产人妻一区二区 | 亚洲欧美综合在线观看 | 久久久三级 | 婷婷色一区二区三区 | 国产在线导航 | 99午夜 | 免费福利视频网站 | 美女草逼视频 | 色戒在线免费 | 日韩一区二区三区不卡 | 欧美激情在线免费观看 | 第一av| 日韩国产欧美视频 | 亚洲成年人专区 | mm131丰满少妇人体欣赏图 | 中文字幕日韩三级片 | 日韩一区二区三区电影 | 久久久久中文 | 欧美少妇bbw | 在线免费av网站 | 免费看女生隐私 | 日本国产精品 | 少妇精品视频 | www.狠狠| 91在线观看高清 | 调教小屁屁白丝丨vk | 黄色片在线视频 | 久久久久成人精品无码 | 日韩欧美不卡 | 美日韩在线 | 欧美巨大荫蒂茸毛毛人妖 | 国内毛片毛片毛片 | 欧美少妇xxxx| 91在线精品一区二区 | 久久久久久影视 | 亚洲男女啪啪 | 日韩精美视频 | 视频在线免费观看 | 狠狠操在线视频 | 波多野结衣小视频 | 激情91| av老司机在线 | 手机在线免费看av | 岛国精品在线 | 青青草久久久 | 欧洲在线视频 | 国产h视频在线观看 | 国产极品久久久 | 女同互舔视频 | 国产精品午夜福利 | 在线观看网页视频 | 国内自拍偷拍视频 | 色综合久久网 | 午夜视频福利在线观看 | 久久一二三四 | 欧美色偷偷 | 色屁屁网站 | 国产日韩欧美高清 | 高h视频在线播放 | 亚洲精品日韩av | 日韩在线一区二区三区四区 | 美女一区二区视频 | 999久久久久| 人人插人人舔 | www.色综合.com| 性生活视频免费观看 | 男男play呻吟动漫网站 | 亚洲精品久久久久avwww潮水 | 亚洲小视频在线观看 | 99热这里只有精品9 欧美一级网 | 浮力影院国产第一页 | 中文字幕精品一区久久久久 | 国产高清网站 | 2019中文在线观看 | 欧美私人影院 | 91看片网站| 九九色视频 | 日本第一页 | www日本视频 | 国产视频久久久久久久 | 国产成人久久精品 | 久久久久久综合 | 国产欧美一区二区精品忘忧草 | 国产成人一区二区三区 | 午夜在线影院 | 少妇媚药按摩中文字幕 | 黄色高潮视频 | 日韩成人在线网站 | 丰满少妇被猛烈进入30p | 天天艹夜夜艹 | 少妇视频免费 | 久久久久成人精品无码 | free性丰满4khd性欧美 | av电影一区| 成人h视频在线观看 | 成年女人毛片 | 日韩淫片| 3d肉腐团 | 免费a在线 | 日本一区二区免费视频 | 黄色不卡 | 西方裸体在线观看 | 久久国内视频 | 理伦在线 | 欧洲美女屁股眼交3 | 公和我乱做好爽添厨房中文字幕 | 久久久精品网 | 小受受扒开屁股挨网站 | 色接久久 | 爱情岛论坛亚洲品质自拍 | 天堂网亚洲| 夜夜干天天操 | 天天超碰 | www色中色 | 免费a网站 | 欧美一级艳片视频免费观看 | 欧美视频在线观看免费 | 日本精品视频一区 | 邻家有女4完整版电影观看 www.久草.com | 91精品国产综合久久久蜜臀 | 天天超碰 | 日韩国产精品一区 | 天天爽天天摸 | 日韩黄色一级片 | 亚洲免费一区 | 姐妹 5 | 极品嫩模炮交高潮叫床喷液 | 欧美日韩国产中文字幕 | 日日cao| 狠狠婷婷 | 午夜生活片| 51免费看成人啪啪片 | 九色91在线 | 国产精品扒开腿做爽爽 | 久久久久久久av | 国产视频久久久久久久 | 在线观看av网站 | 精品成人在线 | 91精品国产综合久久久久久 | 黄色高潮视频 | 天天操比 | 京香视频 | 在线天堂资源 | 日韩中文字幕一区二区三区 | 成人涩涩| 久久久噜噜噜久久久 | 性欧美又大又长又硬 | 热99精品| 亚洲欧洲在线播放 | 国产人妻精品一区二区三区不卡 | 精品中文字幕在线观看 | 91青青操| 欧美疯狂做受xxxxx高潮 | 色哟哟入口国产精品 | 91福利院| 国产成人一区二区三区 | 久久午夜夜伦鲁鲁一区二区 | 国产专区一 | av激情网站 | 欧美天天影院 | 欧美日韩一区二区午夜 | 久久久久在线 | 国产白浆视频 | 老师露出强行让男生揉动漫 | 午夜怡红院 | 亚洲欧洲日韩 | 久久精品7| 蜜桃成人在线观看 | 亚洲精品乱码久久久久久久久久久久 | 男女视频在线观看免费 | 亚洲综合另类 | 同桌伸进内裤揉到高潮嗯啊 | 日本护士毛茸茸体内精 | 久久久噜噜噜久久久 | 日本少妇性高潮 | 女m被s玩胸虐乳哭着求饶 | 午夜天堂av | 超碰97免费在线 | 麻豆av免费看| 成人在线观看网站 | 欧美亚洲专区 | 亚洲无人区码一码二码三码的含义 | 黄a在线 | 色国产在线 | 男生和女生一起差差差视频 | 无码视频在线观看 | 精品人伦一区二区三区 | 色狠狠av | 一区二区不卡在线 | 久久久久久久久久免费视频 | 国产在线第一页 | 国产精品夫妻自拍 | 国产精品午夜福利 | 99re在线观看| 日视频| 成人涩涩| 欧美日b视频 | 国产精品久久久久久久成人午夜 | 成人日韩精品 | 特级黄色录像 | 日本高清不卡一区 | 熟妇人妻av无码一区二区三区 | 国产精品自产拍高潮在线观看 | 公和我乱做好爽添厨房中文字幕 | 黄色漫画网站 | 韩国三级hd两男一女 | 亚洲a视频 | 香蕉视频官网 | 国产精品视频久久久久久久 | 日韩精品视频免费播放 | 波多野结衣一区在线观看 | 视频1区 | 扒开女人内裤猛进出白浆 | 深夜福利你懂的 | 女女同性高清片免费看 | 在线91| 泡妞wwwwxxxx | 久久久久无码精品国产 | 超碰夜夜 | 五月深爱| 被闺蜜玩sm(女绑女) | 欧洲美女屁股眼交3 | 一卡二卡在线 | 毛片女人 | 日韩国产精品一区 | 日韩不卡免费视频 | 黄色不卡 | 天天操夜夜操 | 午夜伦伦 | 姐妹5免费观看完整 | 小宵虎南在线观看 | 少妇媚药按摩中文字幕 | 免费播放av | 欧美理伦少妇2做爰 | 内衣办公室第一集 | 久久另类ts人妖一区二区 | 国产精品爽 | 欧美色图首页 | 日韩在线不卡 | 青青草视频在线观看免费 | 91资源在线免费观看 | 奇米影视在线播放 | 中文字幕二区三区 | 天天摸天天舔 | 日韩午夜av | 国产白浆视频 | 999小视频| 好男人在线视频www 中文字幕日韩三级片 | 欧美卡一卡二 | 亚洲综合免费视频 | 日本污污网站 | 久久久com | 96日本xxxxxⅹxxx70| av自拍网 | 一级片a级片 | 黄色三级视频 | 久久久久在线视频 | 电视剧h文肉版 | 天堂网在线观看视频 | 91精品久久久久久综合五月天 | 日韩欧美不卡 | 大黑人巨大荫蒂大交女人 | 日韩专区欧美专区 | 超碰av网 | 巨乳的诱惑 | av在线播放网址 | av一区二区三区在线观看 | 国产又粗又猛又黄又爽无遮挡 | 成年视频在线 | 亚洲h片 | 一二三四av| 罗宾被到爽高潮痉挛 | 午夜影院免费观看 | 性黄色小说 | 啊灬岳灬啊灬快灬高潮了 | 日韩精品专区 | 视频一区欧美 | 波多野结衣在线一区二区 | 亚洲成人av在线电影 | 国产综合第一页 | 国产无套精品一区二区 | 日日夜夜免费精品视频 | 欧美特级黄 | 国产一区91精品张津瑜 | 一级美女视频 | 你懂的国产 | 免费一区二区在线观看 | 国产在线观看第一页 | 又黄又骚的视频 | 激情小说激情视频 | 欧美成视频 | 娇妻被朋友强得嗷嗷叫 | 亚洲成人精品视频在线观看 | 色噜噜一区二区三区 | 亚洲人xxx日本人18 | 制服.丝袜.亚洲.另类.中文 | 日本三级不卡 | 亚洲午夜免费视频 | 国产精品日韩精品 | 日本xx视频 | 日本高清有码 | 高清一区二区三区 | 1985美国式禁忌4 | 国产精品欧美精品 | 免费毛片大全 | 中文字幕观看在线 | 九九视频在线播放 | 久久88| 久久综合激情网 | 中文字幕啪啪 | 五月天婷婷丁香花 | 中文字幕视频观看 | 人人澡人人干 | 美国av片 | 同人动漫在线观看 | 成人久久精品人妻一区二区三区 | 欧美视频一区二区三区四区 | 香蕉午夜 | 九九精品九九 | 日本一区二区三区视频在线观看 | 成人黄色av网站 | 亚洲熟女乱色综合亚洲小说 | 激情综合激情五月 | 男人肌肌桶女人肌肌 | 黄色网址在线免费观看 | 无人在线免费观看视频 | 一本加勒比hezyo黑人 | 60岁老太做爰 | 女人的呻吟声 | 中国毛片直接看 | 日视频 | 国产一区二区三区免费视频 | 黄色网址入口 | 另类一区二区三区 | 亚洲视频777 | 国产在线一级 | 欧美疯狂做受xxxxx高潮 | 天天干夜夜欢 | 成人看片免费 | 日韩精品www | 婷婷在线视频观看 | 中文字幕久久网 | 黄色a网站 | 青青草原国产 | 69婷婷国产精品入口 | 成人av亚洲 | 久久精品一区二区三区四区 | 91成人免费网站 | 中文字幕无产乱码 | 日韩中出 | 国产福利电影在线观看 | 久久久久成人精品无码 | 一区二区免费在线观看 | 双性人hdsexvideos | 亚洲欧美a | 青娱乐国产 | 日本精品中文字幕 | 大奶子影院| 成人免费看片视频 | 人妖视频网站 | 亚洲精品乱码久久久久久 | 精品国产aⅴ一区二区三区东京热 | 制服.丝袜.亚洲.中文.综合懂 | 深夜成人福利视频 | 嗯灬啊灬快灬高潮了 | 天天操好逼 | 国产一区二区三区四区视频 | 欧美激情一区二区 | 99久久精品国产一区二区三区 | 林由奈在线观看 | 欧美a级在线观看 | 亚洲理论视频 | 日韩精品久久久久久 | 欧美精品一级二级三级 | 青青草一区 | 免费在线观看毛片 | 西方裸体在线观看 | 男人猛吃奶女人爽视频 | 污网站免费观看 | 精品国产乱码久久久久久郑州公司 | 蜜桃一区二区三区 | 久久麻豆精品 | 日视频| 天天操人人 | 五月亚洲综合 | 免费福利视频网站 | 国产精品边吃奶边做爽 | 中文字幕欧美激情 | 久久久久久国产视频 | 精品看片| 免费观看xxx在线观看下载 | 国产免费久久 | 久久天天躁狠狠躁夜夜躁2014 | 国产456| 天天插插插| 免费看片网站91 | 九九小视频| 麻豆一二区 | 亚洲一区在线观看视频 | 高h喷水荡肉爽文1v1沉芙 | 另类第一页| 国产一区二区视频免费 | 91视频观看 | 免费观看黄网站 | av在线入口 | 久久久久女人精品毛片九一 | 四虎在线免费视频 | 国产精品午夜影院 | 91成人在线 | 久久久久久综合 | 免费性网站 | 嫩草影院在线观看视频 | 久久精品2 | 午夜资源 | 亚洲爱色 | 少妇av一区二区三区 | 一级片黄色录像 | 美国一区二区 | 四虎av网站 | 又色又爽又黄gif动态图 | 出轨的女人高潮叫床视频网站 | 高清中文字幕在线a片 | 男女涩涩视频 | 四虎永久免费 | 精品国产乱码久久久久 | 免费观看在线高清 | 99久久精 | 国产激情在线观看 | 免费a网站 | 新香蕉视频 | 91蝌蚪网| 欧美9999| 91爱视频| 中文在线免费 | 久免费一级suv好看的国产 | 妇女主任大腚耸动着 | 操在线视频| 国产做a爰片aaaaaoooo | 亚洲第一大网站 | 亚洲一区二区久久 | 武则天一级淫片高清免费观看 | 黄色网战| 柔嫩的麻麻下面好紧 | 在线观看国产成人 | 少妇性l交大片7724com | 爱爱中文字幕 | 欧美一及片 | 亚洲综合伊人 | 成人福利网址 | 另类专区亚洲 | 亚洲三级免费 | 国模一二三区 | 女人扒开腿免费视频app | 亚洲精品一区二区三区在线 | 日韩精品午夜 | 久久国产成人 | 九九黄色片 | 超碰男人的天堂 | 日韩女优在线观看 | 免费观看日批视频 | 婷婷一二三区 | 久久久www | 亚洲国产一区二区波多野结衣 | 日韩电影在线一区 | 亚州精品国产精品乱码不99按摩 | 久久久成人av | 精品不卡一区 | 99热这里只有精品5 综合久久久久久久 | 亚洲aa | 日韩午夜在线观看 | 日韩欧美福利视频 | 999精品视频| 天堂中文字幕在线观看 | gogo人体做爰大胆视频 | 成人黄色在线观看 | 日本精品中文字幕 | 天堂成人av | 成人深夜网站 | 四虎影视在线 | www.激情| 永久免费,视频 | 色撸撸在线视频 | 999小视频| 日韩欧美色图 | 99久草| 亚洲乱码国产乱码精品 | 故意穿暴露被强好爽 | 在线观看亚洲欧美 | 日本一区二区三区在线免费观看 | 大学生av| 91高清免费视频 | 在线观看日韩 | 嫩草嫩草嫩草嫩草嫩草嫩草 | 国产一卡二卡三卡 | 超碰在线98 | 91视频在线免费观看 | 免费色网站 | 欧美午夜精品久久久久久人妖 | 成人av手机在线观看 | 爱豆国产剧免费观看大全剧集 | 欧美在线观看一区二区 | 少妇献身老头系列 | 国产又爽又黄免费视频 | 色哟哟av| 欧美人禽交 | 日本免费福利视频 | 丰满女邻居的色诱4hd | 欧美性一区二区三区 | 亚洲熟妇无码久久精品 | 色噜噜在线观看 | 九九精品九九 | 91theporn国产在线观看 | 日韩一区二区三区电影 | 国产尤物在线 | 天天舔天天射天天干 | 网站黄色片 | 精品久久久精品 | 欧美人与性动交g欧美精器 国产91在线播放精品91 | 人妻丰满熟妇av无码久久洗澡 | 欧美黄色特级片 | 91麻豆精品国产91久久久更新资源速度超快 | 越南黄色片 | 蜜桃成人av| 美女大黄动图 | 成人福利网址 | 精品国产成人 | 亚洲精品在线观看视频 | a√天堂在线 | 国产无人区码熟妇毛片多 | 精品国产乱码久久久久 | 女人久久 | 国产精品熟妇一区二区三区四区 | 高清一区二区三区 | 国产99久久九九精品无码免费 | 99re这里| 国产午夜一级一片免费播放 | 精品啪啪 | 日韩欧美亚洲一区二区三区 | 日韩精品视频免费播放 | 国产精品18岁 | 啊啊啊轻点疼视频 | 操操操免费视频 | 亚洲二区视频 | 强行伸进她的小内裤疯狂揉摸视频 | 在线aaa | 黄色高潮视频 | 欧美丰满老熟妇xxxxx性 | 人妖视频网站 | 精品看片 | 高潮失禁喷水颤抖哭叫视频 | 国产一卡二卡三卡 | 亚洲三级黄 | 国内一区二区 | 亚洲国产欧美另类 | 欧美视频一区二区 | 亚洲制服丝袜av | 黄色污污视频在线观看 | avapp在线观看| 美国毛片基地 | 一边摸内裤一边吻胸 | 欧美做受69 | 久久99久久99 | 国产尤物在线 | 午夜精品久久久久久久99热浪潮 | 亚洲视频在线免费播放 | 色哟哟中文字幕 | 日韩免费一区二区 | 国产一区二区三区四区视频 | 国产小视频免费在线观看 | 四虎在线观看视频 | 欧美熟妇另类久久久久久不卡 | 沈悦高志欣 沈镇南原著小说 | 亚洲av中文无码乱人伦在线视色 | 手机av免费在线观看 | 久操av在线 | 香蕉视频在线网站 | 快播视频在线观看 | 久久天堂影院 | 性色av蜜臀av色欲av | 国产视频二 | 神马久久精品 | 日本一区二区三区在线免费观看 | 国产精品久久久久久99 | 欧美激情视频一区二区三区 | 黄色wwww| 内衣办公室第一集 | 色视频免费观看 | 91av视频| 午夜日韩 | 一级黄色网址 | 久久久久久精 | 日本黄色动态图 | 波多野结衣av在线观看 | 国产精品2018| 中文字幕一二区 | 色偷偷综合 | 国产精品久久久久久久久久久久久久久久久久 | 国产456| 免费观看国产视频 | 在线国产精品视频 | 国产精品久久久久久久妇 | 亚洲成人精品一区二区 | 成人小视频免费观看 | 日韩亚洲在线 | 欧美粉嫩metartvideo | 日韩一区二区不卡 | 亚洲精品在线观看视频 | 黄色草莓视频 | 国产午夜精品视频 | 好看的毛片 | 综合色播 | 亲嘴激烈床视频大全床 | 中文字幕成人在线 | 欧美黄色大片在线观看 | 国产日韩在线播放 | 成人av福利| 后宫流全肉h文艳文 | 欧美激情第二页 | h文网站 | 国产做受高潮动漫 | 日本韩国在线观看 | 免费欧美视频 | 日韩成人免费观看 | 亚洲视频一区二区 | 97毛片| 亚洲国产网站 | 五月综合视频 | avtt中文字幕 | 男人捅女人网站 | 亚洲综合色网 | 亚洲人视频 | 深夜福利视频导航 | 亚洲av中文无码乱人伦在线视色 | 粉嫩久久99精品久久久久久夜 | 好男人在线视频 | 国产微拍精品 | www.17c.com喷水少妇 | 欧洲亚洲一区二区三区 | 啊啊嗯视频 | 亚洲免费片 | 欧美日韩一二 | 一级理论片 | 欧美疯狂做受xxxxx高潮 | 国产精品视频无码 | 国产午夜在线视频 | 色视频导航 | 婷婷看片 | 大尺度做爰呻吟舌吻 | 欧美丰满老熟妇xxxxx性 | 日韩中文字幕在线观看视频 | 美日韩在线| 国产精品天天狠天天看 | 日本高清xxx | 51av在线| 丁香六月| 91禁蘑菇在线看 | 精品日韩欧美 | 国产美女明星三级做爰 | 欧美一区二区区 | 久久精热| 天天爱天天做 | 久久久久精 | 亚洲一页 | 国产真实乱人偷精品人妻 | 午夜免费毛片 | 男女涩涩视频 | 久免费一级suv好看的国产 | 国产一区二区三区四区在线观看 | 亚洲av无码片一区二区三区 | 完美搭档在线观看 | 久久天堂影院 | 99re在线精品视频 | 日本丰满熟妇videossex | 免费成人短视频 | 成人久久精品人妻一区二区三区 | 另类少妇人与禽zozz0性伦 | 高清中文字幕在线a片 | 爱情岛亚洲品质自拍极速福利网站 | 啊用力嗯轻一点 | 久久久噜噜噜 | 天天天天躁天天爱天天碰2018 | 视频一区欧美 | www.国产免费 | 中文字幕第35页 | 欧美三区 | 国产黄色一区 | 狠狠鲁视频 | 日韩性片 | 亚洲一区在线播放 | 国产精品久久久久久妇女6080 | 日本精品一区 | 国产三级在线免费观看 | 成年黄色网 | 美女视频网址 | 99久久国| 播放毛片 | 日韩精品一区二区三区高清免费 | 色综合激情 | 超碰av网 | 激情欧美一区二区 | 国产美女免费视频 | 亚洲二三区 | 国产精品一区二区三区在线播放 | 日韩精品久久久久 | 黄色片欧美| 人人爽爽人人 | 羞辱狗奴的句子有哪些 | 精品国产乱码一区二区 | 精品黑人一区二区三区在线观看 | 欧美人与动物xxx | 国产全肉乱妇杂乱 | 日韩精品一区二区三区四区五区 | 亚洲一区中文字幕在线观看 | 成人免费福利 | 成年人av| 青青草草 | 高潮失禁喷水颤抖哭叫视频 | 久久久久久精 | 欧美中文字幕在线视频 | 四虎四虎| 出轨的女人高潮叫床视频网站 | 东方影库av | 看看毛片 | 卡一卡二视频 | 精品国产乱码久久久久久郑州公司 | 成人久久久精品乱码一区二区三区 | 在线免费高清 | 国产激情av| 在线日本中文字幕 | 久久久天堂国产精品女人 | 国产日韩欧美视频 | 欧美日韩一区二区三区在线 | 国产乱码77777777 | 成人福利网址 | 今天高清视频在线观看 | 亚洲videos| 欧美大片91 | 电视剧h文肉版 | 精品人妻av区 | 九色视频偷拍少妇的秘密 | 日韩中文字幕视频 | 成人精品在线播放 | 潘金莲三级80分钟 | 奇米影视888 | 米奇影音 | 亚洲一级网 | 天天狠天天操 | 亚洲欧美日本另类 | 天堂毛片 | www.av网站 | 自拍视频网 | 中文字幕黑人 | av在线试看| 丝袜天堂| 性黄色小说 | 天天操好逼 | 成人18视频在线观看 | 69婷婷国产精品入口 | 久久天天躁狠狠躁夜夜爽蜜月 | 成人福利网址 | 女人扒开腿免费视频app | 日韩不卡视频在线 | 中文天堂av | 国产麻豆精品视频 | 亚洲AV无码精品自拍 | 午夜宅男影院 | 性色av蜜臀av色欲av | 欧美大片免费看 | free性video法国极品 | 娇bbb搡bbbb揉bbbb | 久久99久久99精品蜜柚传媒 | 91theporn国产在线观看 | 手机av免费 | 色男av | 欧美黄片一区二区三区 | 麻豆av影院| 福利视频在线导航 | 免费看av的网址 | 爱情岛亚洲首页论坛 | 午夜伦情 | 日韩免费在线播放 | 91精品久久久久久综合五月天 | 国产一区二区精品丝袜 | av不卡网| 亚日韩在线 | 亚洲一区小说 | 亚洲天堂中文 | 国产欧美久久久久久 | 深夜福利你懂的 | 国产伦精品一区二区三区 | 丰满女邻居的色诱4hd | 亚洲午夜久久久久久久久红桃 | 国内毛片毛片毛片 | 精品久久久av | 丰满人妻熟女aⅴ一区 | 欧美一级片网站 | 婷婷激情小说 | 脱了内裤互相蹭很舒服 | 亚州高清| 在线视频 日韩 | 精品看片| 成人动漫视频在线观看 | 黄色91在线观看 | 天天操比 | 在线视频第一页 | 欧美大片一区二区 | 亚洲欧美自偷自拍 | 《办公室高潮秘书 | 欧美日韩视频一区二区 | 538国产精品一区二区免费视频 | 国产深夜福利 | 91麻豆精品国产91久久久更新资源速度超快 | 欧美xxx视频 | 云缨被到爽高潮痉挛 | 国产激情影院 | 伊人激情综合 | 免费观看在线高清 | 人成在线视频 | 日本黄色免费网址 | 毛片网页| h双腿涨灌触手play慎入视频 | 日本久久久久久 | 国产精品短视频 | 日韩一级二级三级 | 一级黄色网址 | 国产男男gay| 牛牛电影国产一区二区 | 天天cao| 贱奴张开腿给主人打烂 | 精品午夜福利在线观看 | 粗大的内捧猛烈进出 | 在线日本中文字幕 | 免费无遮挡无码永久在线观看视频 | 久久黄色网络 | 国产精品无码在线播放 | 久久久精品人妻无码专区 | 香蕉网在线视频 | 欧美视频在线观看一区二区 | 噼里啪啦高清 | 欧美福利社| 日本h片 | 一区二区三区四区亚洲 | 亚洲精品水蜜桃 | 久久偷看各类女兵18女厕嘘嘘 | 电视剧h文肉版 | 午夜激情网址 | 中文字幕精品一二三四五六七八 | 波多野结衣视频在线播放 | 国产精品成人免费 | av小说天堂网 | 亚洲精品欧洲精品 | 中文字幕专区 | 国产综合在线视频 | 日韩在线亚洲 | 污网站在线看 | 中文字幕mv| www.av在线.com | 交换配乱淫东北大坑性事视频 | 免费观看黄色大片 | 黄色小说软件 | 免费观看黄色大片 | 狠狠干天天射 | 人人爽爽人人 | 精品99久久 | 久久55 | 疯狂欧美大伦交乱 | 亚洲午夜免费视频 | 精品尤物blackedhd | 日日撸夜夜操 | 日本中文字幕在线播放 | 91福利在线观看 | 亚洲 激情 小说 另类 欧美 | 欧美a级在线观看 | 漂亮的岳hd中文字幕 | 30一40一50老女人毛片 | 中文字幕一二三区 | 先锋成人资源 | 欧美疯狂做受xxxxx高潮 | 日本asian农村少妇pics | 中文亚洲欧美 | 久久久久噜噜噜亚洲熟女综合 | 国产成人无码www免费视频播放 | 日韩a级片 | 自宅警备员在线观看 | 黄色伦理电影 | 九色91在线 | 国产无人区码熟妇毛片多 | 一区二区日韩精品 | 欧美日本另类 | 黄页网站免费观看 | 成人教育av | 一边亲嘴一边做好爽视频 | 亚洲视频一区二区 | 久久精品高清 | 色播激情网 | 另类五月天 | 亚洲av成人无码一二三在线观看 | 欧美一性一乱一交一视频 | 国产福利电影在线观看 | 女生叉开腿让男生捅 | 狠狠爱天天干 | 你懂的日韩 | 欧美36p| 人妻丰满熟妇av无码久久洗澡 | 一区二区福利视频 | 午夜窝窝| 熟妇人妻av无码一区二区三区 | 黄色精品网站 | 免费的av网址 | 国产第一页在线观看 | 日韩午夜在线观看 | 国产99久久九九精品无码免费 | 2019中文在线观看 | 日韩一区欧美 | 阿v免费视频 | 人妖被c到高潮欧美gay | 献给魔王伊伏洛基亚吧动漫在线观看 | 在线中文字日产幕 | 欧美丰满老妇 | 欧美人体做爰大胆视频 | 波多野结衣伦理 | 超碰公开免费 | 日本午夜免费 | 操操影视 | 男的艹女的视频 | 又黄又骚的视频 | 亚洲激情 | 久久精品久久精品 | 久久伊人网站 | 日本精品人妻无码77777 | 九九精品国产 | 中文免费视频 | av在线官网 | 免费成人短视频 | 中国黄色一级片 | 国产1页 | 91九色视频在线观看 | 经典一区二区三区 | 国产精品久久久久久无人区 | 在线观看中文字幕码 | 精品尤物blackedhd | 极品女教师裸体瑜伽视频 | 国产精品久久九九 | 自拍毛片 | 国产精品自拍一区 | 看免费毛片 | 性黄色小说 | 91亚洲国产精品 | 国产一区二区影院 | 男女做那个视频 | 久免费一级suv好看的国产 | 亚洲精品一区二区三区四区高清 | 日韩欧美不卡 | 五月婷婷视频在线 | 99精品久久久 | 成人中文字幕+乱码+中文字幕 | 波多野结衣av电影 | 天天操天天摸天天干 | 亚洲一区二区自偷自拍 | 欧美草比| 中文字幕理论片 | 国产色区 | 国产极品久久久 | 亚洲日本va | 姐妹5免费观看完整 | 99热这里只有精品2 欧美一二三区视频 | 久久精品片 | 91tv国产成人福利 | 女性向av| 四虎黄色片 | 91视频精品 | 激情小说激情视频 | 亚洲日批| 天堂网亚洲 | 同桌伸进内裤揉到高潮嗯啊 | 天堂中文字幕在线观看 | 欧美激情视频在线播放 | 成人交配视频 | 国产精选第一页 | 国产一区二区三区欧美 | 91丨porny丨在线中文 | 成年人性生活片 | 丰满人妻熟女aⅴ一区 | 视频在线观看一区二区 | 久操视频在线免费观看 | 日韩亚洲在线 | 我和岳交换夫妇爽4p晓娟小说 | 久久麻豆精品 | 国产精品自产拍高潮在线观看 | 色老头影视 | 91正在播放| 国产精品无码免费播放 | 一本不卡| 黄视频网站在线观看 | 亚洲一区人妻 | 色播开心网 | 啊室友轻点h总攻 | 日韩精品自拍 | 白色白色在线视频 | 五月婷婷六月激情 | 欧美一级网| 另类尿喷潮videofree | 少妇肥臀大白屁股高清 | 久久中文视频 | 日韩久久中文字幕 | 西方裸体在线观看 | 老色鬼网站 | 国产欧美精品在线 | 91久久久久久久久 | 久久精品午夜 | 国产精品入口久久 | www五月天com | 青青草久久久 | 天天爽天天摸 | 国内自拍偷拍 | 精品国产麻豆 | 精品国产乱码久久久久久郑州公司 | 天堂成人av | 中国黄色一级片 | 麻豆电影在线观看 | 久久视频这里只有精品 | 亚洲拍拍| 超碰狠狠干 | av青青| 人人插人人澡 | 一边亲嘴一边做好爽视频 | 久久神马| 美女主播福利视频 | 中国特黄一级片 | 上原亚衣在线观看 | 欧美激情综合色综合啪啪五月 | 做爰全过程叫床视频 | 九九久久精品视频 | 亚洲激情成人网 | 婷婷啪啪 | 在线天堂中文在线资源网 | 免费黄色网址大全 | 俄罗斯黄色大片 | 中文天堂| 丰满少妇被猛烈进入30p | 脱了内裤互相蹭很舒服 | 裸体女人a级一片 | 亚洲一区二区三区三州 | 国产高清小视频 | 国产精品三 | 欧美福利视频网 | 亚洲综合网站 | 天天射影院 | 中文在线观看视频 | 精品欧美黑人一区二区三区 | 午夜精产品一区二区在线观看的 | 中文字幕3页 | 国产一级做a爰片在线看免费 | www.好了av | 欧美极品少妇xxxxⅹ喷水 | 电影《色戒》无删减版 | 日韩黄色一级片 | 男人和女人日b视频 | www.17c.com喷水少妇 | 成年人在线观看免费视频 | 三上悠亚被淫辱の教室下载 | 婷婷一二三区 | 他摸着我下面突然伸进去了视频 | 亚洲国产一区二区波多野结衣 | 国产精品高潮呻吟久久久 | 综合另类| 同桌伸进内裤揉到高潮嗯啊 | 欧美黑人添添高潮a片www | 国产免费麻豆 | 色哟哟入口 | 人妻无码一区二区三区免费 | 高h视频在线观看 | 日日干日日操 | 泰国午夜理伦三级 | 中出在线观看 | 蜜桃黄网| 久久99久久99 | www男人天堂 | 国产入口| 亚洲精品久久久久avwww潮水 | 《巨乳女教师》bd版电影 | 亚洲 激情 小说 另类 欧美 | 成人黄色免费网站 | 国产精品成人免费看片 | 东方影库av| 日韩一本 | 久久久久久蜜桃 | 我和岳交换夫妇爽4p晓娟小说 | 亚洲全黄 | 在线a天堂 | 国产一区二区麻豆 | 国产精品一区二区三区在线播放 | 久久久久噜噜噜亚洲熟女综合 | 成人激情视频网 | 裸体女人a级一片 | 男女啪啪小视频 | 免费中文字幕在线观看 | 久久九九久久九九 | 亚洲清纯唯美 | 中文在线免费 | 国产中文字幕在线播放 | 97精品久久 | 二级黄色大片 | 亚州av综合色区无码一区 | 香蕉视频免费在线观看 | www.日日| 日韩视频一二三 | 97视频精品 | 三年免费高清大全电影 | 女仆扒开让客人玩 | 狂野欧美性猛交xxxx巴西 | www.日日 | 国产ts丝袜人妖系列视频 | 韩国av网 | 最近2019中文字幕大全第二页 | 最新的黄色网址 | 中文字幕mv | 黄色激情小说视频 | 丁香花五月天 | 日本三级免费看 | 一级免费在线观看 | 国产ts系列| 五月婷婷综合在线 | 大学生三级中国dvd 三级黄色短视频 | 午夜三级视频 | 91禁蘑菇在线看 | 黑人一级片 | 亚欧色 | 黄色片在线视频 | 日韩精品无 | 日韩在线视频不卡 | 超碰最新网址 | 日少妇b | 欧美性伦理 | 在线免费视频 | 日本三级视频在线 | 成人h视频在线观看 | 曰本黄色大片 | 成人在线高清 | 好男人网站 | 免费中文字幕 | 波多野结衣在线观看一区 | 日韩每日更新 | 韩国三级丰满少妇高潮 | 香蕉视频在线网站 | 欧美大片在线 | 国产一区二区三区视频在线播放 | 日韩一卡二卡 | 天天激情 | 伊人国产精品 | 中文字幕观看在线 | 男人天堂a | 99久久九九| 无人在线免费观看视频 | 福利视频在线导航 | 九九99| 欧美bbbbbbbbbbbb18av | 欧美黄色片 | 神秘电影永久入口 | 又大又长粗又爽又黄少妇视频 | 狂野欧美性猛交xxxx巴西 | 亚洲免费一区 | 姐姐8免费完整高清电视剧在线看 | 韩国一区二区三区四区 | 亚洲一区二区三区三州 | 亚洲欧美日韩色图 | 我和单位漂亮少妇激情 | 熟女毛毛多熟妇人妻aⅴ在线毛片 | 俺去啦最新网址 | 免费毛片大全 | 日本中文字幕在线播放 | 国产午夜在线视频 | 欧美一级特黄视频 | 在线播放免费av | 久草婷婷 | 日本骚少妇| 亚洲av永久中文无码精品综合 | 欧美一二三级 | 免费看污片网站 | 男人j捅女人p | 制服.丝袜.亚洲.中文.综合懂 | 性福直播 | 日本一区二区精品视频 | 成人在线观看网站 | 青青草免费公开视频 | 晚上碰视频| av导航在线观看 | 九九热精品在线 | 国产一区二区三区在线观看 | 色综合图片 | 爱豆国产剧免费观看大全剧集 | 久久另类ts人妖一区二区 | 羞羞漫画在线登录页面免费漫画入口页面cnmo | 黄色一级网站 | 羞辱狗奴的句子有哪些 | 上原亚衣在线观看 | 亚洲综合日韩 | 亚洲免费在线 | 69热在线观看 | 久久偷看各类女兵18女厕嘘嘘 | 国产资源视频 | 国产九区 | 亚洲爱av| 亚洲免费片 | 日韩成人精品一区二区 | 九九九九九精品 | 国产精品人人 | 潘金莲激情呻吟欲求不满视频 | 写真福利片hd在线播放 | 鲁视频| 情趣调教喷水h | 超碰在线播 | 欧美极品一区二区 | 欧美视频在线观看免费 | 爱爱视频免费网站 | 男人免费网站 | 激情文学88 | 下一站婚姻全集免费观看 | 色黄网站在线观看 | 猛男gaygay免费网站漫画 | 凸凹视频在线观看 | 免费色网 | 柔嫩的麻麻下面好紧 | 97av视频在线 | 欧美色精品天天在线观看视频 | 日本在线网址 | 插入阴道视频 | 午夜激情在线视频 | 蜜桃成人免费视频 | 姐妹5电影高清全集在线观看免费 | 成年网站在线观看 | 男生和女生一起差差差视频 | 黑白配av| 欧美黄色特级片 | 神马久久精品 | 制服丝袜国产在线 | 中文字幕理论片 | 99国产精品一区 | 琪琪久久 | atv在线观看免费播放 | 制服丝袜国产 | 女女同性高清片免费看 | 伊人网大香 | 触手动漫 | 91成人免费网站 | 天堂成人av | 夜夜骚av一区二区三区 | 欧美视频免费在线观看 | 91视频黄色 | 99免费观看视频 | 色视频免费观看 | 夜夜夜影院 | 丰满少妇被猛烈进入 | 精品视频在线播放 | 娇小6一8小毛片 | 毛片电影院 | 打屁股无遮挡网站 | 欧美三级一区二区三区 | av在线播放网站 | 成人国产一区二区 | 亚洲视频久久 | 爆乳熟妇一区二区三区 | 久久久久久久久久一区二区三区 | 深夜福利免费在线观看 | 大尺度做爰呻吟舌吻 | 色婷婷欧美 | 国产精品探花视频 | 国产精品久久久久久久久久妞妞 | 少妇一边喂奶一边我做 | 欧美色精品天天在线观看视频 | 被夫上司蹂躏的七天七夜在线观看 | 亚洲美女久久久 | 国产精品久久久久久妇女6080 | 你懂的国产在线 | 美日韩免费视频 | 51av在线| 蜜桃视频污 | 91成品视频 | 日本变态折磨凌虐bdsm在线 | 亚洲一区中文字幕在线观看 | 91在线一区| 日韩免费观看 | 亚洲一区二区免费看 | 国产精品久久久久久久久久久久久久久久久久 | 性日本xxx | 日本三级网| 日韩一二三四五区 | 娇bbb搡bbbb揉bbbb | 一级二级毛片 | 强伦女教师2 | 国产一级免费视频 | 日韩色图在线观看 | 欧美黑人添添高潮a片www | 嫩草精品| 99re这里 | 美女被草网站 | 日韩av免费网站 | 国产成人小视频 | 日本91av | 性生活一级视频 | 麻豆精品一区二区三区视频 | 强行伸进她的小内裤疯狂揉摸视频 | 操操影视| 考逼视频| 色综合天天综合网天天狠天天 | 黑人和白人做爰 | 欧美一区二区三区视频在线 | www.日本黄 | 波多野结衣在线电影 | 自拍视频网 | 在线观看网页视频 | 国产免费一区二区三区在线观看 | 中文字幕精品一区久久久久 | 久久人人精品 | 一本加勒比北条麻妃 | 日韩精品一区二区三区高清免费 | 女人高潮叫床骚话污话 | 成人深夜视频 | 68日本xxxxxⅹxxx22 | 麻豆视频免费版 | 国产原创视频在线观看 | 男人j捅女人p | 久热精品视频在线观看 | 色综合图片 | 麻豆精品在线 | 粗了大了 整进去好爽视频 日韩一区二区三区电影 | 大奶在线观看 | 久久久久噜噜噜亚洲熟女综合 | 成人久久久精品乱码一区二区三区 | 第四色成人网 | 欧美人体做爰大胆视频 | 另类一区二区三区 | 国产一区二区三区四区在线观看 | 久久久精品999| 日韩中字在线 | 女仆淫院 | 日韩中文字幕高清 | 亚洲一区人妻 | 欧美色图在线观看 | www日本在线观看 | av2017天堂网 | 久久神马 | 一个人在线观看www 97成人资源 | 相亲对象是问题学生在线观看 | 国语对白av| 久久久777 | 女人裸体又黄 | 窝窝午夜看片 | 免费看成人毛片 | 好大好爽好舒服 | 他揉捏她两乳不停呻吟视频 | 综合色av | 在线观看国产精品入口男同 | 黄频在线观看 | 国产小视频在线看 | 亚洲欧美日韩色图 | 窝窝午夜看片 | 波多野结衣在线观看 | 日本黄色网址大全 | 我和几个阿的性事 | 他揉捏她两乳不停呻吟视频 | 亚洲色女| 男女拍拍视频 | 久久综合av | 免费国产a | 国产成人综合视频 | 日本黄色免费观看 | 最新女另类z000z000 | 白丝女仆被免费网站 | 神马久久久久久久久 | 欧美又大又粗又长 | 欧美黄色一级视频 | 在线看黄色片 | 亚洲成人av一区二区三区 | 日韩欧美亚洲一区二区三区 | 手机av免费在线观看 | 日韩大片在线观看 | 日韩欧美一区二区三区在线观看 | 西方裸体在线观看 | 国产一区二区三区四 | 天天综合永久入口 | 亚洲精品一区二区三区区别 | 美女aaa| 亚洲一区中文字幕在线观看 | asian成熟肉图pics| 丝袜美女视频网站 | 浮力影院国产第一页 | 姐脱你看 | 啪啪自拍 | 国产又大又黄又爽 | 免费观看黄 | 两个男人躁一个女人免费视频 | 日本精品一区 | 成人福利免费视频 | 91麻豆精品国产91久久久更新资源速度超快 | 一区二区三区精品视频 | 美日韩一区二区 | 我的丝袜美腿尤物麻麻 | 午夜影院操 | 日韩丰满少妇 | 亚洲一区电影 | 亚洲另类视频 | 国产精品扒开腿做爽爽爽男男 | 麻豆传媒在线观看 | 久章草影院 | 免费看av的网址 | 国产污视频 | 两个男人躁一个女人免费视频 | 在线观看麻豆视频 | 日本裸体女优 | 日韩jizz | 少妇被按摩师摸高潮了 | 贱奴张开腿给主人打烂 | 在线中文字幕av | 久久久久女人精品毛片九一 | 婷婷激情综合网 | 国产二区视频在线观看 | 国产特级毛片aaaaaa | 国产高潮流白浆 | 天堂婷婷 | 故意穿暴露被强好爽 | 伊人欧美 | 亚洲欧美另类在线视频 | 少妇2做爰bd在线意大利堕落 | 伊人青青草原 | 日日操视频 | 黑白配av| 奇米影视第四色777 狠狠操免费视频 | 亚洲伊人色 | 欧美另类综合 | 狠狠视频| 香蕉影院在线观看 | 欧美日韩电影一区 | 中文字幕人妻一区二区在线视频 | 这里只有精彩视频 | 成人免费无遮挡无码黄漫视频 | 日韩在线视频不卡 | 色人阁婷婷| 男女超碰 | 免费草逼视频 | av不卡网 | 九九久久免费视频 | 可以在线看的av | h在线免费 | 胸大被男同桌强解开胸罩床吻 | 成人精品视频一区二区三区尤物 | 青青草视频 | 欧美三级黄色 | 亚洲国产欧美另类 | 91精品国产综合久久久久久 | 91久久色| 久久久久久成人 | 日本三级精品 | 成人一级黄色片 | 久色精品| 色婷婷久久综合 | 特级西西人体444www高清大胆 | 在线观看亚洲成人 | 91久久久久| 波多野结衣电影av | 日本乱子伦 | 国产中文在线观看 | www.激情| 女帝裸体被吸乳羞画 | 婷婷激情综合网 | 一二三四区在线 | 乱色精品无码一区二区国产盗 | 日本理论片中文字幕 | 成人久久 | 天堂av2014| 精久久久久 | 91麻豆精品国产91久久久更新资源速度超快 | 亚洲精品一区二区在线 | www.激情五月 | 天天操天天弄 | 中国黄色一级片 | 成人h在线观看 | 久久久久噜噜噜亚洲熟女综合 | 国产a三级 | 欧美激情在线免费观看 | 91资源在线免费观看 | 亚洲欧美在线一区 | 日韩精品免费一区二区 | 97精品国产露脸对白 | 色伊人av| 999精品视频在线观看 | 久久久成人av | 性爱视频免费 | 人妻无码一区二区三区免费 | 人人干超碰 | 三级国产在线观看 | 日韩av中文字幕在线播放 | 色屁屁网站 | 美国女孩毛片 | 精品午夜福利在线观看 | 日本成人综合 | 日本在线精品视频 | 欧美嫩交| 91蝌蚪91密月 | 9999国产精品 | 福利视频网址导航 | 久久久久久成人 | 粉嫩aⅴ一区二区三区四区五区 | 黑人黄色大片 | 丝袜脚交国产在线观看 | 欧美第一网站 | 天天激情 | 国产美女免费视频 | 久久久久无码精品国产 | 在线播放你懂的 | 狠狠干老司机 | 一道本无吗一区 | 欧美成人免费 | 日韩欧美国产高清 | 操女人逼逼视频 | 黄色三级在线视频 | 高跟91白丝 | 献给魔王伊伏洛基亚吧动漫在线观看 | 草在线视频| 长篇武侠肉伦小说 | 久久视频在线免费观看 | 黄色精品网站 | 东方影库av| 午夜视频免费 | 午夜黄色在线观看 | 视频在线免费 | 看看毛片| 一曲二曲三曲在线观看中文字幕动漫 | 丰满女邻居的色诱4hd | 午夜精品久久久久久久久久 | 亚洲少妇一区二区三区 | 91秦先生在线播放 | 操你啦av | 瑟瑟综合 | gogogo高清免费播放 | 一本久久综合 | 伊人精品在线 | 日韩久久中文字幕 | 99热日本 | 毛片无限看 | 操女人逼逼视频 | 成人在线高清 | 国产精品一区二区三 | av视屏| 免费看黄色av| 精品动漫一区 | 男操女在线观看 | 91精品免费视频 | 成人欧美精品一区二区 | 99热在线播放 | 日韩av高清在线观看 | 亚欧色| 你懂的在线视频网站 | 亚洲丰满| 美女上床网站 | 制服.丝袜.亚洲.中文.综合懂 | 亚洲国产精品99 | 亚洲人成免费 | 免费在线看黄网站 | 国产美女免费 | 欧美成人精品一区 | 欧美人与禽zozzozzo | 精久久久久 | 东北一级黄色片 | 成人亚洲一区 | 99久久人妻无码中文字幕系列 | 91成品视频 | 一男一女操 | 日本熟妇一区二区三区 | 国产精品资源在线观看 | 黑人黄色大片 | 日韩不卡视频在线 | 久久99精品久久久久久琪琪 | 国产小视频在线看 | 欧美视频一区二区三区四区 | 一本加勒比hezyo黑人 | 欧美大片免费高清观看 | 中文字幕第四页 | 毛片毛片毛片毛片 | 热99精品 | 四川bbb搡bbb爽爽视频 | www.亚洲精品 | 久久久青青 | 又色又爽又黄18网站 | 欧美人吸奶水吃奶水 | 大香焦伊人 | 国产一区二区三区四区精 | 相亲对象是问题学生在线观看 | 欧美激情综合色综合啪啪五月 | 久久中文视频 | 天天插一插| 亚洲国产精品免费 | 国产精品99久久久精品无码 | 欧美视频免费在线观看 | 欧美黄页 | 很嫩很紧直喷白浆h | 国产精品一区二区三 | 99久精品 | 亚洲jizzjizz日本少妇 | 又大又粗又爽18禁免费看 | 色吊丝网站| 国内毛片毛片毛片 | 久久天天躁狠狠躁夜夜躁2014 | 亚洲免费不卡视频 | 在线观看中文字幕网站 | 黄色高潮视频 | 视频在线免费观看 | 亚洲色女 | 中文字幕在线观看线人 | 艳妇乳肉豪妇荡videos | 中文在线观看视频 | 天堂a√在线 | 亚洲成人av一区二区三区 | 天海翼一区 | 99资源| 国产精品一区在线观看 | 乱色精品无码一区二区国产盗 | 天堂99| 亚洲h片 | 牛牛视频在线 | 又色又爽又黄18网站 | 不卡视频在线播放 | 国产精品成人免费 | 91国产大片| 亚洲国产精品久久久久 | 亚洲性xxxx | 中出在线观看 | 日批视频免费看 | 国内精品久久久久 | 日本黄色动态图 | 日韩一级一区 | 亚洲小说区图片区都市 | 凸凹视频在线观看 | 色男av| 亚洲黄色网址 | 波多野结衣av电影 | 黄色wwwww| 成人亚洲 | 天天激情 | 国产激情在线观看 | 日韩国产片 | 激情小说在线 | 欧美激情第二页 | 少妇真人直播免费视频 | 夜夜夜影院| 亚洲视频网站在线观看 | 少妇视频免费 | 久久精品7 | 日本午夜免费 | 小受受扒开屁股挨网站 | 日本一区二区三区在线播放 | 黄色一级片网站 | 久久久久成人精品无码 | 男女啪啪免费网站 | 少妇人妻丰满做爰xxx | 亚洲午夜av久久乱码 | 亚洲免费高清 | 日韩一区欧美 | 免费三级在线 | 日韩成人免费观看 | 在线观看免费大片 | 韩国三级电影中文字幕 | 手机免费看av片 | 深夜爽爽动态图无遮无挡 | 中文字幕理伦片免费看 | 波多野つ上司出差被中在线出 | 在线观看麻豆视频 | 婷婷综合色 | 国产精品成人在线 | 日韩三级在线免费观看 | 五月精品 | 亚洲熟妇无码av | 日韩一级一级 | 91污免费| 一级肉体全黄裸片中国 | 中文字幕日韩三级片 | 波多野结衣av电影 | 午夜在线影院 | 久久久免费av | www亚洲天堂 | 亚洲爽爽网 | 色播基地 | 国产成人91 | 欧美日韩一二区 | 国内精品999| 91在线精品一区二区 | 色久影院 | 日韩爱爱网 | 加勒比色综合 | 亚洲女优视频 | 男男车车的车车网站w98免费 | 欧美妞干网 | xxxx69美国| 日韩成人精品一区二区 | 中文字幕亚洲在线 | 69热在线观看 | 怡红院av在线播放 | 极品少妇一区二区三区 | 久久精品97| 亚洲乱码视频 | 女人久久 | 月色导航 | 麻豆三级 | 99久久久无码国产精品性波多 | 国产男男gay| 无码人妻丰满熟妇精品 | 猛男gaygay免费网站漫画 | 日日操视频| 黄色天堂网| 撸撸在线视频 | 日本黄色动态图 | 成人在线观看一区二区三区 | 中文字幕视频观看 | 草在线视频 | 国产又粗又猛又黄视频 | 欧美视频在线观看免费 | 丰满的女人性猛交 | 亚洲精品国产精品乱码不卡 | 日日碰狠狠添天天爽 | 美国毛片基地 | 国产一区欧美一区 | 美女性高潮视频 | 中文字 | 成年人免费看视频 | 深夜网站在线观看 | 色婷婷久久综合 | 亚洲xx网 | 一级黄色片免费观看 | h在线免费 | 黄色漫画网站 | 免费观看国产视频 | 一区二区三区免费在线观看 | 人人爽人人草 | 欧美福利视频网 | 色综合天天综合网天天狠天天 | 麻豆免费观看 | 亚洲午夜精品久久久久久浪潮 | 中文字幕一区二区在线观看 | 在线观看日韩 | 国产精品久久久久久99 | av资源库 | 姐妹5电影高清全集在线观看免费 | 天天插插插 | av自拍网| 快播视频在线观看 | 97伊人 | 欧美性在线视频 | 99色综合| 非洲黑人狂躁日本妞 | 亚洲在线第一页 | 国产大尺度视频在线观看 | 欧美日韩精品在线 | 国产精品天天狠天天看 | 成年人精品 | 性生活一级视频 | 青青草中文字幕 | 手机免费看av片 | 亚洲精品在线观看视频 | 久久人人爽爽 | 日韩欧美国产高清 | 公交车被多人伦h | 女生叉开腿让男生捅 | 日日爽日日操 | 制服丝袜国产 | 欧美黄色一区二区 | 玖玖色资源 | 欧美嫩交 | 神马久久久久久久久 | 久久精品在线免费观看 | 亚洲激情成人网 | 日韩福利二区 | 亚洲综合影视 | 殴美毛片 | 欧美一区二区三区久久 | 欧美影院 | 成人hd| 玖玖在线 | 色播激情网 | 日本美女三级 | 99久久九九 | 中文字幕一区二区三区四区五区 | 成人aaa| 91高清免费视频 | 日韩av中文字幕在线播放 | 黑丝一区 | 色老头综合网 | 色哟哟一区二区 | aa一级片 | 激情免费网站 | 天堂岛av | 无码人妻精品一区二区三应用大全 | 男人天堂2021 | 岛国一级片 | 久久久久久黄色 | 最新中文字幕在线 | 欧美福利视频网 | 久久亚洲精品小早川怜子 | 免费观看黄色大片 | 男女拍拍视频 | 秋霞午夜电影网 | 超碰在线中文字幕 | 亚洲九九| 黄色av一级片 | 亚洲午夜久久久久久久久红桃 | 国产一级精品视频 | 亚洲AV综合色区无码国产播放 | 日本伦理电影网站 | 女人的呻吟声 | 国内精品视频在线观看 | 日本一区二区免费视频 | 国产欧美日韩综合 | 欧美又大又粗又长 | 国产性生活 | 亚洲久草| 操你啦av | 91视频黄色 | 日韩中字在线 | 国产精品成人免费 | 美女黄色小视频 | 一级片在线观看免费 | 麻豆精品在线 | 999精品视频在线观看 | 天堂中文在线视频 | 日日干日日射 | 欧美性生活xxx | 亚洲视频二 | 播放毛片 | 国产精品一区二区三 | 91网在线观看 | 台湾三级台湾三级dvd影视 | 亚洲欧美另类在线视频 | 亚洲熟妇色自偷自拍另类 | 亚州黄色 | 亚洲综合一二三区 | 尤物一区 | www.成人在线观看 | 羞羞成人漫画入口 | 国产入口 | 蜜桃黄网 | 蓝猫淘气三千问恐龙时代 | 91免费视频播放 | 制服.丝袜.亚洲.中文.综合 | 欧美作爱视频 | 天天综合永久入口 | 国产一区自拍视频 | asian成熟肉图pics | 国产白嫩美女无套久久 | 精品欧美一区二区精品久久 | 91在线| 熟妇人妻av无码一区二区三区 | 国产欧美一级片 | 香蕉视频在线看 | 啪啪免费小视频 | 日本公妇乱偷中文字幕 | 美日韩免费视频 | 99久久久无码国产精品性波多 | 久久aⅴ无码av高潮av喷吹 | 少妇精品偷拍高潮白浆 | 美女福利视频导航 | 午夜精品三级久久久有码 | 久久久久在线视频 | 欧美人与善交大片 | 色姑娘综合 | 欧美激情在线免费观看 | 潘甜甜在线 | 中文字幕欧美激情 | 波多野结衣亚洲 | 久久久久国产视频 | 国产综合在线播放 | 白嫩小受男同打屁股gay3p | free性av麻豆下载 | 老鸭窝成人 | 日韩精品一区二区三区高清免费 | 欧美午夜精品久久久久久人妖 | xxxx泡妞中国老师 | 538在线精品视频 | 性教育av | 91精品国产乱码 | 91扣逼 | 美女尿尿视频 | 91亚洲国产成人久久精品麻豆 | 国产午夜精品一区二区三区视频 | 免费美女视频 | 免费成人看片 | 免费黄色网页 | 国产精品看片 | 国产在线中文字幕 | 日日天天干 | 亚洲国产视频一区 | 无码人妻精品一区二区蜜桃色欲 | 男女操操 | 久久国产香蕉视频 | 国产色视频| 国产精品久久久久久久久久妞妞 | 扒开双腿让70岁老头看 | 天天爽天天做 | 欧美在线免费观看 | 上司出差调教秘书hd | 五十路av | 欧美精品另类 | 草草在线视频 | 99久精品 | 欧美aaaaaa | 台湾三级台湾三级dvd影视 | 欧美日韩国产中文字幕 | 看片地址 | 视频区图片区小说区 | 色播5月天| 欧洲亚洲一区二区三区 | 天天操天天干天天操 | 草在线视频 | 色播导航 | 国产av无码专区亚洲a∨毛片 | 色一情一乱一伦一区二区三区 | 日韩不卡免费视频 | 国产无套精品一区二区 | 调教撅屁股啪调教打臀缝av | 男女做羞羞的视频 | 亚洲免费不卡视频 | gay男互凵gay男同偷精 | 色噜噜在线观看 | 欧美乱操| 在线观看国产成人 | 久草婷婷 | 在线视频亚洲 | 亚洲欧美日本另类 | 麻豆视频免费版 | 看一级片 | 欧洲黄网| 欧美成人一区二区三区在线观看 | 日本一本在线 | 国产欧美精品在线 | 啊啊啊快高潮了女视频 | 一级精品视频 | www亚洲天堂 | 开心激情播播 | 台湾a级片 | 天海翼一区| 国久久| 欧美爽爽爽 | 亚洲精品久久久久中文字幕二区 | 日韩爱爱网 | 爽天天天天天天天 | 国产一级免费视频 | 国产一区二区三区四区视频 | 天天操人人 | 亚洲一级网 | 名校风暴在线观看免费高清完整 | 国产视频一二区 | 日韩中文字幕 | 夫妻精品 | 欧美激情区 | 亚洲欧美综合网 | 亚洲 欧美 日韩 在线 | 日本免费黄色网 | 久久久精品人妻无码专区 | 成人日韩精品 | av不卡网 | 精国产品一区二区三区a片 快色视频 | 国产伦理网站 | 午夜精品一二三区 | 日本黄色小视频 | 91麻豆精品国产91久久久更新资源速度超快 | 中文字幕一区二区三区四区五区 | 亚洲天堂2024 | 日本三级人妇 | 91成人免费网站 | 精品人妻少妇嫩草av无码专区 | 欧美性猛交xx | 在线观看av网站 | 看看毛片| 3d肉腐团 | 黄页网站免费观看 | 日韩一区免费 | 偷啪自啪 | 国产1页 | 午夜国产一区 | 日韩电影一二三区 | 内衣办公室第一集 | 午夜日韩 | 中文字幕无码人妻少妇免费 | 天天爱夜夜做 | www.国产视频| 欧美日韩中文 | 粉嫩aⅴ一区二区三区四区五区 | 久久亚洲精品国产 | 亚洲色图欧美另类 | 日韩不卡视频在线 | 痞子gay大猛—xnxx2 | 日韩不卡视频在线 | 五月婷婷丁香 | av导航网| 婷婷激情综合 | 在线免费av网 | 日本一区二区三区在线免费观看 | 午夜电影免费看 | 国产专区一 | 黄色精品视频 | 强行伸进她的小内裤疯狂揉摸视频 | 热99精品 | 美女污网站 | 久久精品视频99 | 国产黄色一区二区三区 | 91动画| japanese胖熊gaysextv | 一区二区少妇 | 日本久久久久久 | 97人人射 | 污网站免费观看 | 亚洲小说区图片区都市 | 伊人五月天 | 久久久久久一区 | 日韩精品久久久久久久酒店 | 熟女毛毛多熟妇人妻aⅴ在线毛片 | 久久国产精品免费视频 | 美女黄色小视频 | 日韩精品久久久久久久 | 最近2019中文字幕大全第二页 | 999热视频| 爱情岛亚洲首页论坛 | 成人在线观看一区二区三区 | 亚洲最大黄色 | 成人免费激情视频 | 被夫上司蹂躏的七天七夜在线观看 | 玩有奶水的岳怀孕 | 污片免费在线观看 | 国产三级电影网 | 裸体女人免费视频 | 偷偷在线观看免费播放电视剧大全 | 国内自拍视频在线观看 | 亚洲人成免费 | 色久影院| 99热这里只有精品2 欧美一二三区视频 | 久久国产免费视频 | 午夜影院黄色 | 国产精成人 | 成人亚洲综合 | 中文日韩字幕 | 67194国产| 亚洲拍拍 | 熟妇人妻av无码一区二区三区 | 不卡日韩 | 国产第五页 | 国产99久久久国产精品成人免费 | 91香蕉国产在线观看软件 | 黄色片欧美 | 国产精品久久九九 | 综合色播 | 亚洲综合小说 | 亚洲爱爱视频 | 亚洲一区av在线 | 国产男同gay男男麻豆 | 日韩永久免费视频 | 青青99 | 中文字幕视频 | 日韩精品久久久久 | 国产美女一区二区三区 | 国产又粗又爽视频 | 欧美日韩一区二区三区在线电影 | 韩国三级电影播放 | 久久一二三四 | 在线成人亚洲 | 精品午夜福利在线观看 | 国产精品高潮呻吟久久久 | 亚洲激情一区 | 黄色精品网站 | 免费网站成人 | 亚洲成人7777 | 99久久国 | 日本乱子伦 | 欧美 日本 一区 | 思思在线视频 | 毛片h| 中文无码日韩欧 | 漂亮的岳hd中文字幕 | 亚洲色p| 欧美成视频 | 丰满人妻熟女aⅴ一区 | 啊灬快c我灬啊灬用力灬啊灬 | 少妇精品 | 无码人妻精品一区二区蜜桃色欲 | 麻豆蜜桃91 | 少妇媚药按摩中文字幕 | 骑骑夜电影在线观看免费播放 | 国产精品一区二区三区在线播放 | 国产成人高清 | 日本a级在线 | 国产在线导航 | 五月天激情开心网 | 国产片网站 | 日本一区二区三区在线免费观看 | 污片免费在线观看 | 进去里视频在线观看 | 国产日韩视频在线观看 | 国内自拍视频在线观看 | 91高清免费视频 | 极品嫩模炮交高潮叫床喷液 | 亚洲成人7777| 免费激情视频网站 | 亚洲成人三区 | 成人一区二区三区在线 | 草草在线视频 | 欧美爽爽爽 | 99在线播放视频 | 成人在线观看一区二区三区 | 亚洲精品免费在线观看 | 久久久在线观看 | 男女操操 | 亚洲免费不卡视频 | 揄拍自拍 | 一级特黄aa大片欧美 | 中文字幕综合在线 | 色婷婷久久综合 | 天堂网在线观看视频 | 中文字字幕在线 | www.久草.com | 特级毛片在线观看 | 亚洲精品久久久久中文字幕二区 | 欧美巨大荫蒂茸毛毛人妖 | 无码国产精品高潮久久99 | 欧美日韩久久久 | 国语久久 | 极品女神无套呻吟啪啪 | 精品香蕉一区二区三区 | 日韩三级久久 | 在线成人亚洲 | 日韩爱爱视频 | 五月激情视频 | 揄拍自拍| 成年人免费视频网站 | 中文字幕视频观看 | 国产一级二级三级视频 | 亚洲激情久久 | 99久久久成人国产精品 | 欧美亚洲激情 | 亚洲经典av | 国产高潮视频在线观看 | 色婷婷基地 | 亚洲一区二区三区视频 | 日韩三级久久 | 久久精品在线免费观看 | 永久免费无码av网站在线观看 | 岛国av一区二区 | 欧美另类v | 好看的中文字幕 | 天堂av一区| 久久久精品人妻无码专区 | 黄色动漫在线免费观看 | 97超碰资源站| 久精品视频 | 国产精品午夜电影 | 国产区免费 | 精品福利在线观看 | 少妇被躁爽到高潮无码人狍大战 | 秋霞啪啪片 | 精品在线播放 | 亚洲第一页在线观看 | 日韩人妻无码一区二区三区 | 国产免费大片 | 国产99久久九九精品无码免费 | 波多野结衣一二三区 | 日本三级视频在线观看 | 日韩高清网站 | 国产片91| 久久99精品久久久久久琪琪 | 奇米久久久 | 欧美日韩中文 | 精国产品一区二区三区a片 快色视频 | 双腿打开揉弄高潮 | 欧美六区 | 亚洲999 | 涩涩99| 国产农村av | 成年人的免费视频 | 日本成人在线免费观看 | 丰满少妇被猛烈进入无码 | 好男人在线视频 | 国产精品久久久久久久成人午夜 | 九色91在线 | 爱爱视频免费网站 | 午夜三级视频 | 免费黄污网站 | 京香视频 | 欧美视频免费在线观看 | 午夜视频黄 | 精品久久久久久久 | 中国xxxxxxxxx| 国产999在线观看 | av在线收看| 欧美激情视频在线 | 日本美女三级 | 俺也去av | 免费欧美视频 | 99热播 | 美利坚合众国av | 亚洲精品乱码久久久久久 | 国产国产国产 | 天天躁日日躁狠狠躁av麻豆 | 老牛嫩草二区三区观影体验 | gogogo高清国语完整 | 人妻中文字幕一区二区三区 | 伦理片中文字幕 | www.免费av| 人妻精品久久久久中文字幕69 | 高潮毛片又色又爽免费 | 日本做爰全过程免费看 | 亚洲伊人成无码综合网 | 人人妻人人澡人人爽人人欧美一区 | 三级三级久久三级久久18 | 亚洲免费观看高清 | 99性趣网 | 极品女教师裸体瑜伽视频 | 久久九色| 猛男裸体xvideoscom | 精品国产va久久久久久久 | 老司机福利院 | 色涩综合 | 少妇肥臀大白屁股高清 | 黄在线观看 | 免费中文字幕 | 91亚洲成人 | 999久久久久 | 日本xx视频| 97毛片| 中文字幕第四页 | 91香蕉污视频 | 中文字幕一区二区三区四区五区 | 草莓视频黄app | 亚洲香蕉 | g点强制高潮惩罚 | 欧美aaaaaa| 欧美成人激情 | 亚州av片| 在线免费观看日韩av | 自宅警备员在线观看 | 午夜国产精品视频 | 国产精品国产a级 | 娇妻被肉到高潮流白浆 | 北条麻妃一区二区三区免费 | 中文字幕欧美激情 | 精品黑人一区二区三区 | 中文字字幕 | 五月天在线观看 | 亚洲毛片在线 | 黄色网战 | 成人免费网站视频 | 欧美在线影院 | 不卡影院| 久久久久色 | 国产免费大片 | 成人激情综合网 | 毛片小网站 | 蜜桃视频网站18 | 国产伦精品一区二区三区 | www色中色 | 免费中文字幕在线观看 | 视频在线观看一区二区 | 日本高清xxx | 国产妞干网 | 国产精品1 | 这里只有精彩视频 | 波多野吉衣一区二区 | 视频一区日韩 | 国产精品91视频 | 综合网亚洲 | 久久久久久久久久免费视频 | 中文字幕理伦片免费看 | 国产精品99久久久精品无码 | 91九色视频在线 | 日韩三级在线免费观看 | 成人久久精品人妻一区二区三区 | 毛色毛片 | 小鲜肉gay无套 | 香蕉视频在线免费 | 少妇高潮露脸国语对白 | 国产精品伦子伦免费视频 | 一本久久综合亚洲鲁鲁五月天 | 亚洲精品国产av | 在线aaa | 91色在线观看 | 亚洲精品一区二区三区区别 | 美丽的姑娘国语视频 | 国产传媒av | 久久免费视频观看 | 成人黄色在线视频 | 国产伦精品一区二区三区 | 亚洲欧美日本另类 | 国产手机av| 黄色一级网站 | 亚洲蜜桃精久久久久久久久久久久 | 国产精品88 | 波多野结衣日韩 | 成人福利网址 | 五月婷婷激情综合网 | 欧美大片在线 | 99re这里都是精品 | 国产精品自产拍高潮在线观看 | 久久久久久9999 | 《给我播放》免费观看 | 日本成片网 | 黄色一级片网站 | 欧美日韩国产中文字幕 | 国产视频一区在线观看 | 国产三级三级在线观看 | www色中色| 另类国产 | 午夜秋霞 | 蜜臀av免费 | 人人爽人人草 | 黑白配在线观看免费观看 | 欧美一区二区三区久久 | 林由奈在线观看 | 狠狠鲁视频 | 扣扣文化传媒官网 | 国产精品影音先锋 | 国产视频久久 | 国产视频一区二区 | 国产入口 | 超碰97av| 中国白嫩丰满人妻videos | 国产传媒视频在线观看 | 嗯~啊~快点死我视频在线看 | 三级免费黄 | 国产精品日韩精品 | free性满足hd性video | 女同互舔视频 | 毛片a级片 | 色哟哟入口国产精品 | 人妻丰满熟妇av无码久久洗澡 | 夜夜夜操操操 | 超碰资源总站 | 成人一卡二卡 | 毛片官网 | 日韩天堂av | 青青草原免费观看完整版高清视频电视剧 | 美女高潮网站 | 情趣调教喷水h | 一级理论片 | 国产精品无码免费播放 | 成人日韩精品 | 久久久.www | 人人干人人干 | 欧美在线播放 | 综合网激情 | 欧美成人激情 | 欧美三级黄 | 性xxxx18| www狠狠| 国产麻豆传媒 | 四虎在线观看视频 | 亚洲123 | 亚洲精品免费看 | 九九成人 | 成年人精品| 91久久色| 特黄特黄视频 | 一级特黄色 | 老司机免费在线视频 | 久草视频免费在线播放 | 免费观看黄网站 | 成人黄色免费网站 | 射射色 | 国产视频久久久久久久 | 免费三级在线 | 精品欧美一区二区精品久久 | 制服.丝袜.亚洲.另类.中文 | 贱奴张开腿给主人打烂 | 秋霞午夜鲁丝一区二区老狼 | 天天操天天干天天操 | 国产真实乱人偷精品视频 | 丝袜美女被羞羞网站 | 久久亚洲视频 | 久久久噜噜噜久久中文字幕色伊伊 | 天天色影| 毛片h| 91资源在线免费观看 | 玩有奶水的岳怀孕 | 中文字幕精品一二三四五六七八 | 极品美女一区二区三区 | av资源网址 | 色丁香色婷婷 | 亚洲在线视频播放 | 午夜国产片 | 丝袜脚交国产在线观看 | 日韩视频一二三 | 丰满人妻综合一区二区三区 | 亚洲欧美综合网 | 久久一二三四 | 亚洲毛片在线 | 怡红院男人的天堂 | 国产小u女发育末成年 | 日韩一区精品 | 高跟鞋和丝袜猛烈xxxxxx | 超碰天天干 | 久久视频这里只有精品 | 秋霞午夜伦理 | 亚洲欧美另类在线视频 | 亚洲一区中文字幕 | 五月天视频网 | 女m被s玩胸虐乳哭着求饶 | g点强制高潮惩罚 | 日韩精品久久久久久久 | 68日本xxxxxⅹxxx22| 日韩一区二区精品 | 久草婷婷 | 亚洲综合一二三区 | 亚洲一区二区影视 | 日韩电影一二三区 | 在线播放一区二区三区 | 婷婷看片| 《巨乳女教师》bd版电影 | 色撸撸在线视频 | 射黄视频 | 男人免费网站 | 天堂av一区 | 另类第一页 | 91精品久久久久久综合五月天 | 天天爱夜夜做 | 91精品久久久久久久久中文字幕 | 日本男插女| 亚洲成人视屏 | 国产综合在线视频 | 91看片淫黄大片91桃色 | 亚洲一区二区三区三州 | 色老头综合网 | 成人av一区二区三区在线观看 | 男人捅女人视频 | 最美情侣中文第4季 | 在线观看亚洲欧美 | 欧美日韩久久久 | 国产一区欧美一区 | 国产精品电影一区二区 | 爱豆国产剧免费观看大全剧集 | 扣扣文化传媒官网 | 国产精品久久久久久久成人午夜 | mm131丰满少妇人体欣赏图 | 亚洲天天在线 | 男同小说肉文 | 久久久亚洲一区二区三区 | 污污在线| 成人一卡二卡 | 久久久久久久久久一区二区三区 | 午夜黄色在线观看 | 免费激情视频网站 | 91九色视频在线观看 | 国产一区二区麻豆 | 国产精品国产精品 | 美女被入 | 涩涩av| 日韩av中文字幕在线 | 成人黄色免费在线观看 | 一区二区三区四区av | 午夜黄色在线观看 | 特级西西人体444www高清大胆 | 免费看黄色av | 午夜视频福利在线观看 | 国产精品99久久久精品无码 | 国偷自拍第113页 | 凸凹视频在线观看 | 中国一级黄| 中文字幕一区二区三区乱码 | 国产主播喷水 | 《给我播放》免费观看 | 精品视频一区二区 | 日本成人一区二区 | 三级黄网站 | 国产欧美一级片 | 日日骚av | 日韩每日更新 | 波多野结衣在线一区二区 | 99re这里| 日本在线精品视频 | 91素人约啪 | 色噜噜一区二区三区 | 欧美亚色 | 久久裸体视频 | 精品久久国产 | 中文字幕一区二区三区四区五区 | 日韩免费看 | 女人下边被添全过视频 | 欧美性xxxx极品hd满灌 | 超碰成人97 | 日韩片在线观看 | 欧美黄色大片在线观看 | 青青草原在线免费 | 老师露出强行让男生揉动漫 | av电影在线观看网址 | 波多野结衣在线一区二区 | 在线免费av网 | 亚洲人成免费 | 国内精品999| 嗯啊熟乳岳怀孕好深 | 无码人妻丰满熟妇啪啪网站 | 亚洲区av | 黄色三级在线播放 | 丰满少妇乱子伦精品看片 | 四色永久访问网站 | 蜜桃tv在线观看 | 激情网站在线观看 | 夜晚福利视频 | 9.1人网站免费 | 操欧美大逼 | 全黄一级男人和女人 | 国产男同gay男男麻豆 | 欧美久久精品 | 国产免费一区二区三区在线观看 | 欧美成人激情 | 国产精彩视频 | 91麻豆精品国产91久久久久久久久 | 国产大尺度视频在线观看 | 男女超爽视频 | 麻豆蜜桃91 | 风间由美在线视频 | av高清免费 | 性狂虐xxxxx变态胶衣胶奴视频 | 黑人干亚洲人 | 欧美激情在线免费观看 | 久久高清av | 国产特级毛片aaaaaa | 丁香视频在线观看 | 日韩片在线观看 | 六十路在线观看免费全集高清完整版 | 一区二区在线免费视频 | 黄色片大全 | 看看毛片| 中文字幕人妻一区二区在线视频 | 插吧插吧综合网 | 成人av亚洲 | 国产成人精品免费 | 你懂的国产 | 羞羞成人漫画入口 | 少妇免费直播 | 在线看毛片网站 | 67194国产 | 免费电影av | 日韩成人在线网站 | av毛片在线 | 丰满少妇乱子伦精品看片 | 91亚洲成人| 波多野结衣二区 | 久精品视频 | av福利网站 | 波多野结衣乳巨码无在线观看 | 亚洲欧美自偷自拍 | 日日夜夜免费精品视频 | 3d成人动漫在线观看 | 韩国激情呻吟揉捏胸视频 | 亚洲午夜影视 | 性色av蜜臀av色欲av | 亚洲国产专区 | 放荡的女教师 | 人妻丰满熟妇av无码久久洗澡 | av日日骚 | 欧美激情视频在线 | 色呦呦在线视频 | 丰满女邻居的色诱4hd | 最新女另类z000z000 | 午夜资源| 亚洲啊v在线观看 | 樱桃av | chinese少妇fuce黑人 | 成人性电影 | 三上悠亚被淫辱の教室下载 | 美女国产在线 | 韩国av毛片 | 国产人妻一区二区 | 浮力影院草草 | 成人免费福利 | 成人观看视频 | 永久免费在线视频 | 久久久噜噜噜久久久 | 午夜福利视频 | 午夜国产精品视频 | 丝袜美女视频网站 | 亚洲啪啪网 | 人妻丰满熟妇av无码久久洗澡 | 色撸撸av | 日韩成人免费在线视频 | 国模无码视频一区 | 欧美极品少妇xxxxⅹ喷水 | 久久午夜影视 | 天天草天天射 | 欧美一区2区| 精品国产乱码久久久久久蜜柚 | 午夜精品一二三区 | 香蕉啪啪 | 九九精品视频在线观看 | 男女无遮挡免费视频 | 日本美女一区二区 | 制服下的诱惑暮生 | 综合网亚洲 | 亚洲国产视频一区 | 男人日女人b视频 | 国产欧美二区 | 久免费一级suv好看的国产 | 中文精品在线观看 | 国产男女网站 | 国产网站在线看 | 国产一区二区三区视频在线播放 | 在线综合+亚洲+欧美中文字幕 | 97国产精品久久 | 欧美大片在线 | 麻豆回家视频区一区二 | 床戏做爰摸亲胸视频 | 极品女教师裸体瑜伽视频 | 两个小y头稚嫩紧窄h文 | 一级黄色录像带 | 日韩视频在线一区 | 黄色免费入口 | 爱豆国产剧免费观看大全剧集 | 一级毛片黄色 | 一曲二曲三曲在线观看中文字幕动漫 | 草草在线视频 | 国产原创视频 | sm在线播放 | 亚洲在线第一页 | 亚洲一卡二卡在线 | 国产精品日韩精品 | 公交车上和陌生人做了爱 | 91香蕉污视频 | 天天爽天天摸 | 看片一区| 午夜伦伦 | 国产美女免费 | 四虎永久网址 | 欧美在线性爱视频 | 白丝女仆被免费网站 | www.日韩av.com| 牛牛澡牛牛爽一区二区 | 在线播放av网址 | 亚洲一二三四 | 丰满尤物白嫩啪啪少妇 | 嫩草影院在线观看视频 | 制服丝袜国产在线 | 国产视频久久 | 亚洲免费福利视频 | 99热国内精品 | 国产欧美日韩综合 | 性久久久 | 韩国理伦大片理伦片 | 精品视频一区二区 | 成人一级黄色片 | 91久久精品一区二区三 | 美女张开大腿让男人桶 | 日韩中文字幕在线 | 黄色成人免费视频 | 久久久亚洲一区二区三区 | 日韩精品一区二区三区四区 | 超碰av网 | 香蕉a | 爱情岛论坛亚洲品质自拍 | 国产精品久久久久久精 | 国产视频久久久久久久 | 成人美女视频 | 韩国三级电影中文字幕 | 亚洲伊人成无码综合网 | 日本成人免费观看 | 欧美性生活网 | 欧美在线中文 | 调教撅屁股啪调教打臀缝av | 亚洲国产欧美另类 | 樱井莉亚av | 日韩在线网 | 久久偷看各类女兵18女厕嘘嘘 | 99久草| 亚洲精品色图 | 樱井莉亚av | 触手 侵犯 调教 无尽 | 亚洲尿pisssex撒尿 | 久久黄色录像 | 亚洲77777| 中文字幕一区二区三区乱码不卡 | a√天堂在线 | 三级伦理片在线观看 | 国产精品探花视频 | 91素人约啪 | 欧美在线性爱视频 | 色综久久| 草莓视频黄app| 国内精品免费视频 | 久久精品9 | 久久av资源| 一道本无吗一区 | 非洲黑人毛片 | 三级视频网址 | 久久久精品国产 | 亚洲一级黄色 | 免费观看国产视频 | 亚洲欧美综合网 | 毛片a级片 | 日韩一区二区三区在线视频 | 亚洲免费高清 | 国产精品入口久久 | 很嫩很紧直喷白浆h | 荫蒂被男人添免费视频 | 啊啊啊轻点插 | 毛片无限看 | 久久一区| 欧美不卡影院 | 孕交videos小孕妇xx另类 | 韩国三级电影院 | 免费福利影院 | 在线天堂中文在线资源网 | 亚洲精品欧洲精品 | 久久久久久一区 | 亚洲色图首页 | 日本夫妻性生活视频 | 五月天婷婷网站 | 青青草免费观看 | 黄色三级在线播放 | 韩国激情呻吟揉捏胸视频 | 黄动漫在线观看 | 黑人与日本少妇 | 老师露出强行让男生揉动漫 | 不卡在线| 国产办公室系列 | 不卡av在线播放 | 黄动漫在线观看 | 日韩电影一二三区 | 日韩第1页| 91嫩草欧美久久久九九九 | 亚洲熟女乱色综合亚洲小说 | 少妇在线观看 | 美丽的姑娘国语视频 | 日韩一区高清 | 蜜桃一区二区三区 | 亚洲二三区 | 蜜桃黄网 | 免费观看日批视频 | 国产欧美久久久久久 | 下一站婚姻全集免费观看 | 桃色在线观看 | 国产精品久久av | 黄色草莓视频 | 嗯灬啊灬快灬高潮了 | 国产电影av| 激情亚洲 | 伊人精品在线 | 很污的网站 | 少妇媚药按摩中文字幕 | 欧美国产三级 | 国产精品美女在线观看 | 九九热精品免费视频 | 国产一区二区自拍视频 | 日韩精品999 | 中文精品在线观看 | 同学聚会2交换做爰 | 超碰成人97| 国产一区二区三区四区精 | 99久久久国产 | 女生喷水视频 | 色噜噜一区二区三区 | 亚洲黄色三级视频 | 欧美作爱视频 | 亚洲精品一区二区三区区别 | 亚洲蜜桃精久久久久久久久久久久 | av在线观 | 蜜桃黄网 | 韩国jizz| 亚洲激情成人网 | 国产一区二区三区四区在线观看 | 五十路熟女丰满大屁股 | 调教在线 | 短裙公车被强好爽h吃奶视频 | 久久国语| 亚洲欧洲日韩综合 | 国产在线中文字幕 | 怡红院一区二区三区 | av最新在线 | 日韩av中文字幕在线 | 久久久www | 国产情侣小视频 | 做爰全过程叫床视频 | 天干夜夜爽爽日日日日 | 成人免费看片在线观看 | 亚洲视频二 | 日韩欧美福利视频 | 久久国产主播 | 理论片中文字幕 | 免费视频亚洲 | 亚洲专区第一页 | 欧美精品国产精品 | 成人在线视频网址 | 国产一区二区三区四区视频 | 色撸撸在线视频 | 一二三四区在线 | 欧美少妇xxxx| 粗了大了 整进去好爽视频 日韩一区二区三区电影 | 姐姐8免费完整高清电视剧在线看 | 我的丝袜美腿尤物麻麻 | 国产激情av | 美女脱了内裤喂我喝尿视频 | 调教亲女小嫩苞h文小说 | 啪啪免费小视频 | 日韩美女网 | 性色tv| 日韩女优网站 | 女乡长的太紧太深了在线观看 | 亚州黄色 | 一本大道久久久久精品嫩草 | 国产精品夫妻自拍 | 免费黄色av电影 | 日本久久久久久 | 国产99久久精品一区二区永久免费 | 国产又黄又粗又猛又爽 | 久久人人精品 | 日韩精品极品 | chinese学生高中男gay | 五月天婷婷网站 | av最新天| 人妻熟女一区二区aⅴ水 | 亚洲h片| 日韩中文字幕在线观看视频 | 男生女生啪啪 | 麻豆蜜桃91 | 免费观看在线高清 | 小视频黄色 | 国产精品资源在线观看 | av资源网址 | 两个男人躁一个女人免费视频 | 91亚色在线观看 | 谁有那种在线观看的电影 | 《巨乳女教师》bd版电影 | 国产人妖一区二区 | 久久久久久久久久国产 | 日韩淫片 | 毛片小网站 | 男生桶女生鸡鸡 | 天干夜夜爽爽日日日日 | 五十路熟女丰满大屁股 | 亚洲欧洲在线播放 | 久久国产免费视频 | 丰满少妇被猛烈进入30p | 久久国内视频 | 日韩中文字幕在线观看视频 | 国产一区二区精品丝袜 | 337p粉嫩大胆噜噜噜亚瑟影院 | 日批视频 | 色视频免费观看 | 神马午夜888 | 中文字幕91| 91精品国产综合久久久久久 | 草草视频在线观看 | 在线观看你懂 | 国产精品熟女一区二区不卡 | 日本一级三级三级三级 | 国产精品入口久久 | 国产精品资源在线 | 精品中文字幕在线观看 | 美女露乳| 麻豆入口 | 国产精品久久久久久精 | 在线观看网页视频 | 久久国产一级 | 91豆花视频 | 日本久久99 | 二级片网站 | 看一级片| h文在线观看 | 男人天堂2024| 日韩电影在线一区 | 日本夫妻性生活视频 | 国产精品日韩精品 | 欧美日本免费 | 亚洲激情一区 | 四虎四虎 | 曰批女人视频在线观看 | 熟女毛毛多熟妇人妻aⅴ在线毛片 | 91色交 | 亚洲成人视屏 | 欧美黄色一区二区 | 性色av网站| 一起射导航 | 五月婷婷视频在线 | 欧美视频在线免费 | 国产91福利| 男插女下面视频 | 91九色视频在线观看 | 天干夜夜爽爽日日日日 | 黄色动漫在线看 | 国产1页 | 脱内衣裸身吻胸床戏 | 亚洲一页 | 天天操女人| 欧美另类v| 黑人和白人做爰 | 久久黄色网络 | 热99精品 | 久久另类ts人妖一区二区 | 成人91视频 | 国产69精品久久久久毛片 | 猛男gaygay在线观看 | 日韩中文字幕在线观看视频 | 亚洲欧洲另类 | 少妇av一区二区三区 | 国产系列精品av | 黄色片成人 | 人妻丰满熟妇av无码久久洗澡 | 成人免费一区二区 | 久久av影视| 强行伸进她的小内裤疯狂揉摸视频 | 天干夜夜爽爽日日日日 | 免费a网站 | 日本成人在线免费观看 | 夜夜骚av一区二区三区 | 中文字幕综合在线 | 国产三级伦理片 | 日日干天天插 | 69精品人人人人 | 欧美午夜精品久久久久久人妖 | 欧美大片一区二区 | 久热精品视频在线观看 | 男女插插视频 | 中国女人特级毛片 | 一区二区免费在线观看 | 在线天堂中文在线资源网 | 欧美成人免费观看 | 久久精品动漫 | sleepless动漫在线观看免费播放 精品视频三区 | 精品视频在线播放 | 久久精品动漫 | 亚洲成人www | 美利坚合众国av | 很嫩很紧直喷白浆h | 国产精品免费一区二区三区都可以 | 天天插天天色 | 美丽的姑娘国语视频 | chinese漂亮少妇videos| 亚洲欧美自偷自拍 | 黄页网站免费观看 | 女人天堂网 | 韩国三级电影中文字幕 | 超碰夜夜 | 一男一女在床上拔萝卜 | 男叉女视频 | 一曲二曲三曲在线观看中文字幕动漫 | 九九精品免费视频 | 欧美在线一级片 | 免费中文字幕视频 | 青青草伊人网 | 扣扣文化传媒官网 | 男女av在线 | 禁欲天堂 | 思思在线视频 | 日韩av中文字幕在线播放 | 国产午夜在线观看 | 国产精品99久久久久久久久久久久 | 2020国产在线 | 国产专区一 | 神马久久久久久久久 | 欧美人与性动交g欧美精器 欧美拍拍视频 | 69视频免费观看 | 国产免费一区二区三区在线观看 | 爱操在线 | 99免费观看视频 | 日本在线视频中文字幕 | av在线综合网 | 国产盗摄在线观看 | aa一级片| 国产精品熟女视频 | 丝袜脚交免费网站xx | www.免费av | 日韩毛片在线免费观看 | 99热日本| 特级黄色录像 | 色综合图片 | 香蕉a | 3d肉腐团 | 精品中文字幕在线观看 | 激情文学av | 日韩精品一区二区三区四区 | 精品欧美一区二区精品久久 | 久久精品91 | 国产高清在线观看 | 姐姐8免费完整高清电视剧在线看 | free性中国hd国语露脸 | 狠狠婷婷 | 亚洲另类av | 99国产免费 | 特一级黄色片 | 性色av蜜臀av色欲av | 蓝猫淘气三千问恐龙时代 | 国产一级免费电影 | eeuss电影在线看免费观看 | 国产女处被破www免费 | 黄色一级一级 | 免费av成人| 欧美少妇视频 | 日韩中文字幕有码 | 大尺度舌吻呻吟声 | www日本视频 | 中文字幕人妻一区二区在线视频 | 一级片黄色录像 | 欧美大片免费高清观看 | 成人在线观看网站 | 丰满少妇被猛烈进入30p | 另类第一页 | 粉嫩aⅴ一区二区三区四区五区 | 亚洲天堂成人在线观看 | 国产精品美女在线观看 | 成人av一区二区三区在线观看 | 免费毛片基地 | 天堂岛av| 麻豆回家视频区一区二 | 国产三级在线免费 | 欧美 日本 一区 | 国产精品v亚洲精品v日韩精品 | 91精品久久久久久久99蜜桃 | 四虎av网站 | 亚洲va天堂va欧美ⅴa在线 | 办公室大战高跟丝袜秘书经理ol | 青娱乐国产 | 亚洲欧洲日韩国产 | 午夜天堂av | 五月婷婷视频在线 | 男人肌肌桶女人肌肌 | 波多野结衣不卡 | 丰满熟女人妻一区二区三区 | 日韩免费在线播放 | 欧美午夜影院 | 骚黄网站| 91少妇丨porny丨 | 不卡影院 | 日本三级影院 | 少妇媚药按摩中文字幕 | 日少妇b| www.我爱av | 亚洲乱码中文字幕 | 女人的超长巨茎人妖3d | 亚洲欧美综合在线观看 | 成人久久电影 | 日韩成人午夜电影 | 中文字幕在 | 扒开双腿让70岁老头看 | 午夜精品一二三区 | 色播视频在线观看 | 小十四萝裸体乱喷小说 | 小泽玛利亚一区二区 | 精品国产va久久久久久久 | 福利精品视频 | 国产精品一区在线观看 | 三级黄色短视频 | 甘婷婷全部三级裸体电影 | 亚洲av永久中文无码精品综合 | 岛国一级片 | 久久久久久美女 | www狠狠 | 精国产品一区二区三区a片 快色视频 | 天天色影 | 大桥未久中文字幕 | 亚洲天堂网在线观看 | 自拍偷自拍亚洲精品播放 | 中国一级黄 | 成人一级黄色片 | 一区二区小视频 | 黄视频免费看在线 | 中文字幕无人区二 | 特黄一级毛片 | 午夜精品久久久久久久99热浪潮 | 女人天堂网 | 日韩第九页 | 爆操大奶子| 免费无遮挡无码永久在线观看视频 | 91玖玖 | 亚洲videos | 国产免费播放 | 国产成人无码www免费视频播放 | 男女视频在线观看免费 | 欧美三级电影网址 | 91偷拍网 | 国产又粗又猛又黄又爽的视频 | 激情免费网站 | 电影一区二区三区 | 久久久精品蜜桃 | 日日夜夜精品视频免费 | 姐脱你看| 欧美在线免费视频 | 欧美激情影音先锋 | 污到下面流水的视频 | 性欧美1819性猛交 | 外国毛片 | 91高清视频在线观看 | 人人妻人人澡人人爽精品日本 | 一级片黄色录像 | 亚洲在线视频播放 | 国产人妻一区二区 | 超碰av网 | 国产白嫩美女无套久久 | 亲嘴激烈床视频大全床 | 红桃视频网站 | 国产五十路 | 亚洲欧洲日韩 | 雷电将军裸体 | 国产成人精品自拍 | 二个少妇帮我囗交 | 免费观看xxx在线观看下载 | 五月天激情开心网 | 欧美一级网站 | 日本三级日本三级日本三级极 | 在线国产一区二区 | 强伦女教师2 | 男女插插视频 | 国产深夜福利 | 亚洲欧美国产精品专区久久 | 久草资源站 | 曰韩av| 美女脱了内裤喂我喝尿视频 | 成人在线视频网址 | 国产成人av在线 | 日韩电影在线一区 | 欧美黄色一区二区 | 影音先锋日韩资源 | 国产一级视频 | 国产精品一区二区人妻喷水 | 高h视频在线播放 | 泰国午夜理伦三级 | 欧美最猛性xxxxx(亚洲精品) | 欧美大片高清免费观看 | 国产精品夫妻自拍 | 又污又黄的网站 | 日韩一区欧美 | 韩国深夜啪啪综艺无删减 | 班长露出强行被男生揉 | 献给魔王伊伏洛基亚吧动漫在线观看 | 毛片电影院 | frxxeexxx麻豆hd | 天天躁夜夜躁狠狠躁av | 日本久久99 | 五月婷婷视频 | 性色av蜜臀av色欲av | 娇妻张妍交换高潮 | 丰满熟女人妻一区二区三区 | 夜夜干天天操 | 国产免费一区二区三区在线观看 | 制服丝袜天堂 | 美女脱了内裤喂我喝尿视频 | 91精品国产高清久久久久久久久 | 爆乳熟妇一区二区三区 | 日日干夜夜操 | 日韩一二三四五区 | 免费在线观看毛片 | 综合激情五月婷婷 | 亚洲熟妇无码av | 欧美成人免费观看 | 天堂中文字幕在线观看 | 欧美人与性动交g欧美精器 欧美拍拍视频 | 好看的国产精品 | 日韩欧美色图 | 啊啊啊快高潮了女视频 | 最新中文字幕在线 | 久艹av | 免费看性生活视频 | 人人爱超碰 | 久久精品在线免费观看 | 极品新婚夜少妇真紧 | 91传媒在线播放 | 不卡中文 | 屁屁影院国产第一页 | 黄色激情小说视频 | 住在隔壁的她动漫免费观看全集下载 | 人人草在线视频 | 欧美在线影院 | 欧美草逼网 | 久久综合九色综合欧美狠狠 | 色视频免费观看 | 超碰成人97 | 麻豆传媒在线免费 | 污到下面流水的视频 | 天天操比 | 九色91在线 | 日本久久精品视频 | 国产精品久久久久久久成人午夜 | 少妇被健身教练啪啪 | 国产精品国产精品 | 日本护士毛茸茸体内精 | 四虎在线观看视频 | 香蕉成人app | 91手机在线视频 | 我的好妈妈在线观看 | 国产情侣一区 | 玖草在线| av青青| 天天拍夜夜操 | 国产在线视频卡一卡二 | 男男全程肉无删减电影 | 日韩视频在线一区 | 欧美大片高清免费观看 | 欧美一区二区三区久久 | 少妇裸体视频 | 爱情岛论坛永久入址测速 | 午夜生活片| 中文字幕精品一区久久久久 | 亚洲熟妇色自偷自拍另类 | 成人av观看 | 欧洲三级电影 | 中国白嫩丰满人妻videos | 欧美黄色大片在线观看 | 欧美在线视频免费播放 | 中文字幕视频观看 | av中文字幕在线看 | 在线h网| 亚洲区av | 美女露胸100%无遮挡 | 国产成人无码www免费视频播放 | 丝袜脚交国产在线观看 | 女人的超长巨茎人妖3d | 久久亚洲国产成人精品性色 | 懂色av懂色av粉嫩av分享吧 | 国产一区二区三区视频在线播放 | 91精品国产高清久久久久久久久 | 亚洲熟妇无码久久精品 | 日本黄色动态图 | 少妇一级淫片免费放播放 | 她享受粗啪滋嗯大爷轻点视频 | 精品一区在线视频 | 久久天天躁狠狠躁夜夜爽蜜月 | 亚洲免费观看高清 | 日本在线网址 | 亚洲色图国产精品 | 嗯啊熟乳岳怀孕好深 | 国产精品视频无码 | 日本三级视频在线 | 漂亮的岳hd中文字幕 | 男人捅女人视频 | 裸体喂奶一级裸片 | 日韩影音 | 特及毛片| 国产一区二区三区免费视频 | 国产在线导航 | 国产成人一区二区三区 | 亚洲经典在线 | 国产一区二区三区四区精 | 波多野结衣在线观看 | 在线观看网页视频 | 一区二区三区免费在线观看 | 日韩成人免费在线视频 | 亚洲日本va | 免费观看一区二区三区 | 国产精品熟妇一区二区三区四区 | av先锋资源| 怡红院在线播放 | 免费a在线| 日韩欧美日本 | 波多野つ上司出差被中在线出 | 永久免费成人代码 | 久久久久在线视频 | 欧美一级艳片视频免费观看 | 波多野结衣在线观看一区 | 亚洲精品一区二区三区区别 | 国内毛片毛片毛片 | 日韩永久免费视频 | 91狠狠干 | 欧美日本免费 | 亚洲国产专区 | 日韩欧美黄 | 五月激情视频 | 亚洲AV无码精品自拍 | 亚洲天堂资源 | 短裙公车被强好爽h吃奶视频 | 尤物一区 | 韩国理伦大片 | 欧美在线观看一区二区 | 色接久久| 男女午夜激情 | 泰国午夜理伦三级 | 亚洲狠狠爱 | 无人高清电视剧在线观看直播动漫 | 差差差30分钟 | 国产精品久久久久久久久久久久久久久久久久 | 波多野结衣伦理 | 大尺度av| 免费无遮挡无码永久在线观看视频 | 四虎影视在线 | 中文字幕一区二区三区av | 欧亚av | 91少妇丨porny丨 | 国产丝袜在线视频 | 操到喷水 | 少妇裸体视频 | 中文在线免费 | 1024手机在线观看 | 日韩精品一区二区三区四区五区 | 欧美另类高清 | 67194少妇| 国产一级做a爰片在线看免费 | 亚洲精品1区2区3区 黄色三级图片 | 性视频网 | 久久久久久少妇 | 污的网站 | 国产99久久精品一区二区永久免费 | 九九热在线精品 | 日韩经典av| 日韩每日更新 | 舔的好舒服| 久久精品国产亚洲AV无码男同 | 国产全肉乱妇杂乱 | 名校风暴在线观看免费高清完整 | 国产小视频在线看 | www亚洲天堂| 玖玖爱av | 男女av在线 | 国产精品三| 天天夜夜操 | 三级伦理片在线观看 | 黑白配在线观看免费观看 | 日本污污网站 | 欧美高h | 欧美视频免费在线观看 | 另类少妇人与禽zozz0性伦 | 9.1成人看片| 日本三级视频在线观看 | 好看的中文字幕 | 国产小视频在线看 | 女人高潮叫床骚话污话 | 青青草免费公开视频 | 欧美人与性动交g欧美精器 国产91在线播放精品91 | 日韩午夜av | china18hdxxxx中国| 国产伦精品一区二区三区 | 依人在线 | 麻豆传媒网 | 电视剧h文肉版 | 久草视频播放 | 精品一区二区三区在线视频 | 91正在播放 | 98视频在线 | 51国产偷自视频区视频 | 大黑人巨大荫蒂大交女人 | 福利视频网站 | 日韩精品久久久久 | 免费国产a| 青青青免费在线视频 | 艹男人的日日夜夜 | 精品99久久 | 姐妹5电影高清全集在线观看免费 | 日韩福利二区 | 91最新在线 | 日韩精品一区二区三区四区五区 | 欧美激情综合色综合啪啪五月 | 亚洲av无码片一区二区三区 | 日本中文字幕在线播放 | 国产三级午夜理伦三级 | 亚洲小视频在线观看 | 日韩a | 性狂虐xxxxx变态胶衣胶奴视频 | 男叉女视频 | 91麻豆精品国产91久久久久久久久 | 在线观看中文字幕码 | 欧美簧片在线 | 在线综合+亚洲+欧美中文字幕 | 老师露出强行让男生揉动漫 | 插得好舒服 | 亚洲精品免费在线观看 | 亚洲国产成人综合 | 精品中文字幕在线观看 | 上司出差调教秘书hd | 亚洲videos| 性爱视频免费 | 精品久久久久中文慕人妻 | 嫩草精品 | 在线免费国产 | 九九99| 特级西西人体444www高清大胆 | 91久久精品一区二区三 | 亚洲色图欧美日韩 | 91精品久久久久久综合五月天 | 3d肉腐团| 91视频污版| 国产无套精品一区二区 | 国产精选第一页 | 性xx紧缚网站 | 久草毛片| 福利社av| 欧美一级特黄视频 | 五十路熟女丰满大屁股 | 97色干| 波多野结衣av在线免费观看 | 亚洲最大黄色 | 亚洲中文字幕一区 | 国产毛毛片 | 99久久视频| 亚洲欧洲在线播放 | 日批视频 | 三级黄色av | 久久久久在线 | 色播基地 | www男人天堂 | 国产午夜一级一片免费播放 | 国产99精品视频 | 五月天婷婷丁香花 | 日韩欧美一区二区三区在线观看 | 国产1页 | 大伊人网| 日韩精品一区二区三区四区五区 | 曰本黄色大片 | 日韩毛片中文字幕 | 又大又粗又爽18禁免费看 | 国产av无码专区亚洲av毛片搜 | 免费色网站 | 欧美做受视频 | 福利视频一区二区三区 | 一边亲嘴一边做好爽视频 | 98视频在线 | 亚洲av中文无码乱人伦在线视色 | 欧美日本另类 | 美女尿尿视频 | 欧美亚洲另类在线 | 成人毛片网站 | 黄黄的视频 | 夜夜激情| 爱爱网视频 | 国产乱子伦精品视频 | 看看毛片| 色播导航 | 丁香视频| 日韩欧美一区在线 | 中文字幕成人在线 | 成人福利在线视频 | 7777淫语有声小说 | 美日韩一区二区 | 欧美freesex黑人又粗又大 | 午夜电影一区二区三区 | 九九九九九精品 | 最近更新中文字幕 | 国产欧美在线看 | 第一av| 在线免费av网站 | 爱爱视频免费网站 | 超碰成人97| 国产欧美一区二区 | 一级特黄av| 日韩欧美国产高清 | 久久爱伊人 | 韩国三级hd | 亚洲成人第一页 | 亚洲va天堂va欧美ⅴa在线 | 91在线观看高清 | 国产拍拍视频 | 一级真人毛片 | 久久久精品福利 | 触手 侵犯 调教 无尽 | 玖玖在线免费视频 | 你懂的国产在线 | 国产绿帽一区二区三区 | 日韩欧美亚洲一区二区三区 | 国内精品99 | 丰满少妇乱子伦精品看片 | av福利网站 | 国产成人91| 丝袜天堂 | 神马香蕉久久 | 中文字幕精品一二三四五六七八 | 91超碰网 | 黄色不卡| 日本成人免费观看 | 少妇一级淫片免费放播放 | 国产成人99久久亚洲综合精品 | 91污免费 | 五月婷婷丁香 | 91最新在线| 久久精品在线 | 插入阴道视频 | 毛片av免费看| 欧美日韩一区二区午夜 | 清宫性史3 | 爱爱小视频 | 丰满尤物白嫩啪啪少妇 | 日韩av中文字幕在线播放 | 日本韩国在线观看 | 色一情一乱一伦一区二区三区 | 一本色道久久综合亚洲精品酒店 | 91喷水| 看黄网址 | 香蕉福利视频 | 亚洲欧美另类在线观看 | 奇米久久久 | 欧美在线性爱视频 | 国产一区二区麻豆 | 国产区在线 | 天天干夜夜欢 | 青青草免费观看 | 日本一本不卡 | 日韩在线亚洲 | 久久视频精品 | 少妇人妻精品一区二区三区 | 精精久久 | av不卡网 | 好男人在线视频www 中文字幕日韩三级片 | 国产一区二区三区四 | 《办公室高潮秘书 | 爽交换快高h中文字幕 | 日韩精品午夜 | 亚洲激情 | 亚洲aa| 欧美大片免费高清观看 | 欧美熟妇另类久久久久久不卡 | 午夜67194| 精品欧美一区二区精品久久 | 操操操免费视频 | 韩国一区二区三区四区 | 国产又粗又猛又爽又黄91精品 | 亚洲免费在线 | 伊人成综合网 | 国内自拍偷拍 | 日本一区二区三区在线播放 | 欧美激情xxx| 国产美女一区二区三区 | 北条麻妃一区二区三区 | 精品少妇久久 | 在线你懂的| 六月激情网 | 成年人性生活片 | 外国毛片 | 艳妇乳肉豪妇荡videos | 小十四萝裸体乱喷小说 | 国产黑丝在线 | 午夜视频免费观看 | 国产av无码专区亚洲av毛片搜 | 好吊日在线视频 | 香蕉啪啪 | 九九久久精品视频 | 91精品婷婷国产综合久久竹菊 | 女女百合调教丨vk | 欧美在线影院 | 欧美性生活xxx | 成人av日韩| 影视一区二区三区 | 欧美日韩在线免费 | 亚洲欧洲日韩综合 | 久久无码精品丰满人妻 | 午夜黄色在线观看 | 欧美《交换做爰》电影 | 欧美区日韩区 | 日本美女三级 | 成人在线观看网站 | 扒开双腿猛烈地灌满精子男男 | 欧美性大交| 午夜高清 | 国产午夜福利精品 | 成人国产一区二区 | 日韩性av | 成人一区二区三区在线 | 精品国产乱码一区二区三区 | 国产视频一二区 | 68日本xxxxxⅹxxx22 | 欧美人吸奶水吃奶水 | 毛片直接看 | 国产又粗又猛又黄视频 | 国产一区二区三区四区视频 | 内衣办公室第一集 | 日韩福利电影在线观看 | av在线毛片 | 男人天堂av电影 | 看片一区| 亚洲精品一区二区三区四区高清 | 97伊人 | 一本加勒比hezyo黑人 | 国产精品成人免费 | 交换配乱淫东北大坑性事视频 | 国产成人在线免费 | 欧美嫩交| 久久av一区二区三区漫画 | 这里有精品 | 精品欧美黑人一区二区三区 | 怒海潜沙秦岭神树 | 国产av无码专区亚洲av毛片搜 | 国产原创视频在线观看 | 四川少妇xxx奶大xxx | china18hdxxxx中国 国产黑丝一区 | 妇女主任大腚耸动着 | 一级性生活大片 | 久久永久免费 | 久久天天躁狠狠躁夜夜爽蜜月 | 久久久久在线视频 | 成年人av| 亚洲中文字幕在线观看 | 神马久久久久久久久 | 国产精品国产三级国产 | 国产日韩在线播放 | 在线看成人 | 亚洲福利视频在线 | 谁有那种在线观看的电影 | 图片区小说区视频区 | 无码人妻丰满熟妇啪啪网站 | 阿v免费视频 | 国产精品久久久久久99 | 国产福利电影在线观看 | 欧洲av网站 | 91国产丝袜播放在线 | 免费成人美女女电影 | 国产一区二区三区四区在线观看 | av毛片在线播放 | 久久久成人av | 亚洲色图导航 | 日本一区二区免费视频 | 亚洲尿pisssex撒尿 | 好看的毛片 | 性感少妇av | 奇米狠狠操 | 黄视频免费在线观看 | 日韩在线免费av | 日韩性xxx| 高h校园不许穿内裤h调教 | 午夜视频黄| 四虎在线观看 | 国产一区二区三区四区视频 | 亚洲成人7777 | 亚洲欧美综合网 | 韩国一区二区三区四区 | 女人久久| 天天操人人 | 日韩精美视频 | 久久新视频 | 国产美女免费 | 日本三级免费看 | 贱奴张开腿给主人打烂 | 日本免费福利视频 | 被夫上司蹂躏的七天七夜在线观看 | 麻豆三级 | 大伊人网 | 国产国语性生话播放 | 色人阁av | 夜夜骑天天干 | 国产丝袜av | 日本欧美三级 | 日韩欧美一区二区三区在线观看 | 欧美国产在线观看 | 国产精品扒开腿做爽爽爽男男 | 国产一区二区成人 | 91av视频| 欧洲xxxxx| 精品动漫一区 | 亚洲一区二区三区中文字幕 | 日本人性爱视频 | 成人黄色免费网站 | 欧美激情视频一区二区三区 | 波多野结衣一区二区三区四区 | 性吧av| www.狠狠| 中文字幕av第一页 | 老司机免费在线视频 | 国产男男gay | 欧美午夜精品久久久久久人妖 | 国产ts系列 | 日韩女优在线观看 | 欧美在线视频免费播放 | 成人在线观看一区二区三区 | 欧美区日韩区 | 一级片a级片| 啊用力嗯轻一点 | 亚洲毛片久久 | 国产精品一区二 | 思思精品视频 | 久久偷看各类女兵18女厕嘘嘘 | 女人的呻吟声 | www.激情五月| 疯狂撞击丝袜人妻 | 一区二区在线免费视频 | xxxx69美国| 特级毛片在线观看 | 国产三级精品视频 | 99国产精品一区 | 青青草免费公开视频 | 大尺度av | 亚洲在线第一页 | 精品中文字幕在线观看 | 福利视频一区二区三区 | 99久久九九 | 成人在线高清 | 182tv线路一 成年视频在线观看 | 婷婷深爱五月 | 五月天婷婷丁香花 | 在线综合+亚洲+欧美中文字幕 | 欧美人与禽zozzozzo | 欧美亚洲一区 | 日本一区二区免费视频 | 亚洲黄色成人 | 色妞色视频一区二区三区四区 | 青青操操| 欧美精品中文字幕亚洲专区 | 国产成人精品免费 | 黄色三级在线视频 | 日韩欧美福利视频 | 成年人激情视频 | 插曲免费高清在线观看 | 欧美20p| 中文字幕精品一区久久久久 | 高潮毛片又色又爽免费 | 三级性生活片 | 午夜有码 | 亚洲第一大网站 | 亚洲砖区免费 | 黄色777 | free性中国hd国语露脸 | 欧美日韩不卡在线 | 91亚洲精品国偷拍自产在线观看 | 国产办公室系列 | 亚洲欧美激情视频 | 男女拍拍视频 | 久久人人草 | 免费99精品国产自在在线 | 娇小6一8小毛片 | 狠狠cao日日穞夜夜穞av | 欧美成人精品欧美一级私黄 | 国产成人综合视频 | 写真福利片hd在线播放 | 欧美成人a | 国产精品电影 | 天天超碰| 嗯灬啊灬快灬高潮了 | 草在线视频 | 日日夜夜狠狠干 | 日韩在线观看 | 北条麻妃一区二区三区免费 | 九草在线视频 | 国产男女猛烈无遮挡免费视频动漫 | 成人动漫视频在线观看 | 花样视频污 | 九色视频偷拍少妇的秘密 | 美女爆吸乳羞羞免费网站妖精 | 欧美熟妇另类久久久久久不卡 | 亚洲一级网 | 国产精品mv | 日韩视频在线一区 | 国产一区二区自拍视频 | 欧美一级免费观看 | 成人精品二区 | 亚洲无人区码一码二码三码的含义 | 无码国产精品高潮久久99 | 欧美福利视频 | 亚洲精品一区二区三区四区高清 | 久久无码精品丰满人妻 | 色吊丝网站 | 国产精品操| 啊啊啊轻点疼视频 | 进去里视频在线观看 | 小珊的性放荡羞辱日记 | 国产男女猛烈无遮挡免费视频动漫 | 五月婷婷六月色 | 天堂在线| 四虎影库| 永久免费,视频 | 亚洲激情四射 | 在线爱情大片免费观看大全 | 九九热精品在线 | 中文字幕av第一页 | 亚洲精选一区二区三区 | 99re在线视频| 精品国产乱码一区二区 | 久草资源站 | 欧美第五页 | 女女同性高清片免费看 | 欧美大片91| 亚洲精品乱码久久久久久 | 欧美激情视频在线播放 | 性黄色小说 | 美女黄色小视频 | 性色av蜜臀av色欲av | 亚洲精品一区二区三区区别 | 日本少妇性高潮 | 99久久精品国产一区二区三区 | 无人高清电视剧在线观看直播动漫 | 1024手机在线观看 | 国产情侣小视频 | 插得好舒服 | 看黄免费 | 成人av电影网站 | 在线国产精品视频 | 谁有那种在线观看的电影 | 国产黄片一区二区三区 | 思思在线视频 | 国产男女猛烈无遮挡免费视频动漫 | 椎名空在线 | 日本免费福利视频 | 黑人性视频 | 婷婷在线视频观看 | 精品动漫一区 | 口述我的初苞被强开 | 高潮失禁喷水颤抖哭叫视频 | 91片黄在线观看 | 精品少妇久久 | av小说天堂网 | 视频在线免费观看 | 日本第一页 | 欧美色交 | 国产精品一区二 | 小十四萝裸体乱喷小说 | 欧美三级 欧美一级 | 波多野结衣av在线观看 | 免费黄色av电影 | 亚洲欧美国产高清va在线播放 | 永久免费,视频 | 老司机免费在线视频 | 秋霞二区| 欧美成人免费在线视频 | 短裙公车被强好爽h吃奶视频 | 男男全程肉无删减电影 | 日韩一本 | 日韩a级片 | 乳色吐息在线观看 | 成人欧美精品一区二区 | 91久久电影 | 中文不卡av| 草草在线视频 | 亚洲啊v在线观看 | 永久免费,视频 | 日本国产精品 | 夜夜干天天操 | 三级伦理片在线观看 | 337p粉嫩大胆噜噜噜亚瑟影院 | www.成人在线观看 | 欧洲久久久久 | 日韩中文字幕高清 | 国产特级毛片aaaaaa | 色诱av手机版 | 激情综合激情五月 | 一道本无吗一区 | 深夜福利视频导航 | 免费毛片网站 | 成人观看视频 | 国产视频一区在线观看 | 亚洲人网站 | 曰批女人视频在线观看 | 波多野结衣小视频 | 伊人网大香 | 超碰成人在线观看 | 欧美黄色视屏 | 在线观看三级视频 | 一级特黄色 | 一级片黄色录像 | 伊人精品在线 | 国产精品扒开腿做爽爽 | 天天宗合| 午夜影院免费试看 | 久久久精品网 | 禁欲天堂 | 成年人在线观看免费视频 | 色男av| 国产免费大片 | 中文无码av一区二区三区 | 玩偶姐姐在线观看免费 | 国产成人小视频 | 国产乱国产乱 | 夜夜骑天天干 | 色天天干 | 好吊色视频988gao在线观看 | 麻豆三级 | 小受受扒开屁股挨网站 | 免费的av网站 | 成年人网站在线 | 岛国精品在线 | 天堂av电影| 国产精品v亚洲精品v日韩精品 | 先锋男人资源 | 午夜爱爱网 | 中文字幕麻豆 | 日韩性xxx| 黄色在线 | 国产美女一区二区三区 | 超碰成人在线观看 | 男女网站免费 | 日本免费精品 | 深夜福利你懂的 | 丰满人妻综合一区二区三区 | 久久精品片 | 国产中文字幕在线播放 | 窝窝午夜精品一区二区 | 久久久久久看片 | 日本边添边摸边做边爱 | 这里只有精品9 | 日韩高清精品免费观看 | 国产老女人乱淫免费 | 亚洲av成人无码一二三在线观看 | 天堂av2014| 免费毛片网站 | 91tv在线观看 | 91tv国产成人福利 | 中国一级大黄大黄大色毛片 | 亚洲少妇一区二区三区 | 久久色视频 | 草莓视频网址 | 少妇高潮露脸国语对白 | 精品一区在线视频 | 日韩精品久久久久久久 | 国产丝袜av| 漂亮的岳hd中文字幕 | 日本黄色免费观看 | 一级美女 | 久久久久久久久久国产 | 午夜影院在线观看18 | 国产一区二区三区免费视频 | 欧美在线免费视频 | 久久免费视频网 | 亚洲色图国产精品 | 91精品免费视频 | 日韩特级| 成人观看视频 | h双腿涨灌触手play慎入视频 | aaa在线免费观看 | 最新女另类z000z000 | 日韩在线一区二区三区四区 | 成人黄色在线视频 | 少妇视频在线观看 | 中文字幕在线亚洲 | 欧美做受| 激情夜色 | 一区二区欧美日韩 | 91在线精品一区二区 | 中文字幕一区二区三区四区五区 | 欧美性fee| 女生被男生插 | 麻豆av影院 | 黄色网战 | 久久一区 | 五月婷婷激情视频 | 成人av影视 | 国内毛片毛片毛片 | 中国hd高清xxxxvideo | 无码人妻精品一区二区蜜桃色欲 | 国产九区 | 国产探花一区 | 一区二区精品 | 国产专区一 | 99性趣网 | 国产伦理自拍 | 一区二区福利视频 | 中文字幕精品一二三四五六七八 | 精品香蕉一区二区三区 | 国产精品久久久久久久午夜 | 成人免费在线视频 | 51精品国产 | 娇小tube性极品娇小 | 成人深夜网站 | 免费高清毛片 | 丁香网五月天 | 欧美特级黄色录像 | 日韩影音 | 久久久噜噜噜久久中文字幕色伊伊 | 中国黄色三级 | 精品国产乱码久久久久久蜜柚 | 波多野结衣在线播放 | 视频一区二区在线 | 日批的视频 | 99视频网站| 亚洲h片 | 婷婷九月 | 啊室友轻点h总攻 | a天堂在线观看 | 亚洲精品三区 | 中文字幕精品一区 | 成人黄色免费网站 | 少妇av一区二区三区 | 精品国产乱码久久久久久郑州公司 | 美女露胸100%无遮挡 | 日本成人在线播放 | 国产一区二区三区四 | 日韩欧美国产高清 | 开心色99| 看看毛片| 性爱视频免费 | 福利社av| 啊灬岳灬啊灬快灬高潮了 | 插插插插插插插插插插 | 亚洲乱码中文字幕 | 国产精品人成在线观看免费 | 久久久久久美女 | 女攻总攻大胸奶汁(高h) | 欧美激情第二页 | 天堂网亚洲 | 婷婷看片 | 久久私人影院 | sleepless动漫在线观看免费播放 精品视频三区 | 波多野结衣三级 | 国产精品一区二区三区在线 | 成人精品在线播放 | 国产农村av | 亚洲经典av| 深夜福利片| 91高清免费观看 | 91天堂在线| 国产精品www色诱视频 | 蜜桃综合 | av在线观| 中国女人真人一级毛片 | 欧美人体做爰大胆视频 | 久草综合在线视频 | 亚洲av成人无码一二三在线观看 | 婷婷在线视频观看 | 欧美黄色片 | 久久一二三四 | 亚洲伊人色 | 黄色三级图片 | 亚洲午夜av久久乱码 | aaa亚洲精品 | 黄页网站免费观看 | 一级美女黄色 | 啊室友轻点h总攻 | 欧美三区四区 | 国产高潮视频在线观看 | 黄色a网站| 黄色动漫在线免费观看 | 久久99九九 | 亚洲精品在线观看视频 | 国产精品扒开腿做爽爽爽男男 | 久久国产香蕉视频 | 欧美日韩一二 | 亚洲久久天堂 | 王鸥大尺度做爰未删减 | 男女网站免费 | 亚洲成人第一页 | 中文字幕理伦片免费看 | 故意穿暴露被强好爽 | 快色视频 | 少妇高潮一区二区三区 | 日韩欧美福利视频 | 女乡长的太紧太深了在线观看 | 二个少妇帮我囗交 | 成年视频在线 | 久久黄色录像 | 中文字幕专区 | 国产精品久久久久久妇女6080 | 欧美日韩精品久久 | 久久精品9| www.狠狠 | 天天摸天天舔 | 亚洲精品成av人片天堂无码 | 电视剧h文肉版 | 成年视频在线 | 天天操夜夜做 | 神马久久久久久久久 | 极品少妇一区二区三区 | 日本国产视频 | 少妇一边喂奶一边我做 | 日批视频 | 伊人夜夜躁av伊人久久 | 欧美性xxxx极品hd满灌 | 中国xxxxxxxxx| 在线免费观看日韩av | 亚洲影视一区二区 | 一个人在线观看www 97成人资源 | 色01看片网| 欧美爽爽爽 | 成人免费看片视频 | 九九小视频 | 樱桃av| 久久黄网站 | 先锋成人资源 | 一级少妇女片 | 欧洲女女同性videoso | 啊啊啊啊啊好多水 | 涩涩av| 深夜福利网站 | 亚洲人xxx日本人18 | 精品视频三区 | 开心色99 | 日本高清视频www | 精品一区二区三区免费 | 成年人在线观看免费视频 | 夜间福利视频 | 舔的好舒服 | 国产又粗又猛又爽视频 | www日本在线观看 | 日本精品人妻无码77777 | 京香视频 | 97在线观看视频 | 中国挤奶哺乳午夜片 | 极品女神无套呻吟啪啪 | 黄色片aa| 深爱激情综合 | 亚洲精品国产av | 蘑菇视频hd在线 | 亚洲欧美日韩在线播放 | 极品女教师裸体瑜伽视频 | 色撸撸在线视频 | 婷婷色综合 | 日日干日日射 | 久久久精品免费观看 | 精品女同一区二区 | 高h喷水荡肉爽文1v1沉芙 | 老熟妇精品一区二区三区 | 黄色污污视频 | free性av麻豆下载 | 男人天堂2024 | 图书馆的女友在线观看 | 污污网站在线 | 老牛嫩草二区三区观影体验 | 自拍偷拍p| 亚洲免费毛片 | 久久久久久9 | www.日韩av.com| 欧美精品国产精品 | 在线观看亚洲成人 | av电影日韩 | 精品欧美一区二区三区 | 色久影院| 黄色污污视频在线观看 | 国产精品伦子伦免费视频 | 国产视频一二区 | 中文字幕精品一区久久久久 | 欧美色图在线观看 | 黄色特级片 | 美脚の诱脚舐め脚视频播放 | 被闺蜜玩sm(女绑女) | 日韩不卡视频在线 | 麻豆精品视频 | 日韩无码精品一区二区三区 | 久久久久久黄色 | 91精品久久久久久久99蜜桃 | 国产成人精品在线 | 色哟哟av| 欧美国产日本 | 国产精品电影 | 黄色草莓视频 | 国产高清小视频 | 无码人妻丰满熟妇啪啪网站 | 中文久久乱码一区二区 | 秋霞午夜鲁丝一区二区老狼 | 欧美亚洲专区 | 18国产免费视频 | 色老头综合网 | 亚洲一区小说 | 我想看毛片 | 黄色理论片 | 亚洲天堂中文 | 欧美一区二区三区久久 | 麻豆久久久久久 | 91啪在线| 视频在线观看一区二区 | 久久日av| 成人福利片 | 欧美人吸奶水吃奶水 | free性av麻豆下载 | 国产精品影音先锋 | 97视频精品 | 永久免费在线视频 | 亚洲久草 | 啊用力嗯轻一点 | 在线爱情大片免费观看大全 | av资源库 | 四川bbb搡bbb爽爽视频 | 国产一区二区成人 | 麻豆av电影在线 | 国产午夜精品在线观看 | 久久国产香蕉视频 | 日本久久99 | 日本年轻漂亮大胸继拇 | 思思在线视频 | 国产男男gay| 六月色播| 六月婷婷综合 | 不卡在线| 国产中文字幕在线播放 | 三级伦理片在线观看 | 《给我播放》免费观看 | 日本三级人妇 | 欧美在线免费观看 | 欧美日韩人妻精品一区二区三区 | 国产黄片一区二区三区 | 日本不卡视频在线 | 爆乳熟妇一区二区三区 | 在线观看免费福利 | 浮力影院国产第一页 | 成年人在线观看免费视频 | 成人精品视频一区二区三区尤物 | 国产欧美a | 毛片高清 | 日韩1页 | 二级片网站| 狠狠操在线视频 | 同学聚会2交换做爰 | 胸大被男同桌强解开胸罩床吻 | 午夜18视频在线观看 | 亚洲国产成人久久 | 岛国av一区二区 | 免费成人深夜 | 天堂综合网 | 日韩av一级 | 岛国一级片 | 国产精品, | a天堂资源在线 | 麻豆入口 | 色撸撸av| 欧美猛交免费 | 娇妻秘密进俱乐部穿环调教 | 免费无遮挡无码永久在线观看视频 | 黑人和白人做爰 | 人人妻人人澡人人爽精品日本 | 97人妻精品一区二区三区视频 | 一二三四区在线 | 一区二区小视频 | 短裙公车被强好爽h吃奶视频 | 中文字幕第27页 | 久久久精品影院 | 久色视频在线 | 国产三级午夜理伦三级 | 日日爱网站 | 黄色成人影视 | 泰国午夜理伦三级 | 女女百合调教丨vk | 欧美日韩在线观看视频 | 天天操夜夜操 | 调教亲女小嫩苞h文小说 | 一曲二曲三曲在线观看中文字幕动漫 | 婷婷综合色| 欧美视频一区二区三区四区 | 日韩色综合 | 天天天天躁天天爱天天碰2018 | 久久综合久久鬼 | 色丁香色婷婷 | 国产一区二区自拍视频 | 涩涩的动漫 | 国内自拍偷拍 | 名校风暴在线观看免费高清完整 | 女教师三上悠亚ssni-152 | 国产激情影院 | 国产91在线播放精品91 | 中文字幕第27页 | 黄色网址在线免费观看 | 国产精品久久影视 | 男女视频在线观看免费 | 国产一区二区自拍视频 | 亚洲永久av | 色撸撸在线视频 | g点强制高潮惩罚 | 99热这里只有精品2 欧美一二三区视频 | 午夜av在线播放 | 先锋男人资源 | 欧美极品少妇xxxxⅹ喷水 | 91少妇丨porny丨| 婷婷成人在线 | 粗大的内捧猛烈进出视频 | av福利网站 | 国产永久精品大片wwwapp | 黄色网页在线观看 | a亚洲天堂 | 国内自拍偷拍视频 | 国产白嫩美女无套久久 | 亚洲黄色片网站 | 欧美一区二区三区久久 | 国产视频网站在线观看 | 色撸撸在线视频 | 久久久久久一区 | 亚洲三级黄 | www.五月激情| 韩国三级黄色 | 国产精品第一 | 欧美大片黄 | 视频在线免费 | 久久伊人网站 | 人蛇交高h太爽了h | 在线视频导航 | 亚洲经典av| 国产每日更新 | 岛国av不卡| 小舞被调教成奶奴魅魔视频 | 精品在线免费观看 | 免费v片在线观看 | 男女超爽视频 | 最近2019中文字幕大全第二页 | 日韩成人免费在线视频 | 久久久久伊人 | 精品肉丝脚一区二区三区 | 亚洲最大中文字幕 | 在线观看亚洲欧美 | 精品尤物blackedhd | 写真福利片hd在线播放 | 日本黄a三级三级三级 | 欧美一区二区三区视频在线 | 豆花视频网站 | 亚洲精品乱码久久久久久 | 一级特黄aa大片欧美 | 顶级毛片| 五月开心网 | 久久黄色大片 | 超碰69| 30一40一50老女人毛片 | 91动画| 国产精品久久久久久精 | 欧美三级一区二区三区 | 国产精品无码午夜福利 | 日韩视频在线观看免费 | 性免费视频 | av青青 | 邻家有女4完整版电影观看 www.久草.com | 91麻豆成人 | 天天爱夜夜做 | 日本大尺度做爰呻吟舌吻 | 日本人性爱视频 | 圣女被打开双腿触手调教视频 | 国产精品午夜福利 | 爱情岛论坛永久入址测速 | 成人免费在线视频 | 欧美特黄| 欧美bbbbbbbbbbbb精品 | 蜜桃综合| 黄色特级片 | 91福利视频网 | 国产欧美一区二区 | 欧洲三级电影 | 久久88| 国产一区久久 | 久久久精品国产sm调教网站 | 羞羞成人漫画入口 | 青青草视频 | 亚洲精品www | 国产一区免费视频 | 色噜噜在线观看 | 日本久久久久久 | 国产精品美女毛片真酒店 | 久久国产成人 | 日韩精品久久久久久 | 在线播放你懂的 | 欧美性伦理| 一级做a爱 | 伊人久久综合影院 | 考逼视频 | 四川bbb搡bbb爽爽视频 | 国产精品91视频 | 综合色av | 自拍偷自拍亚洲精品播放 | 色妻av| 中国毛片直接看 | 国产一区二区三区四区视频 | www.伊人网 | 国产原创视频在线观看 | 91亚洲国产成人久久精品麻豆 | 超碰老司机| 白色白色在线视频 | 岛国av一区二区 | 班长露出强行被男生揉 | 欧美丰满老妇 | 久久精品7 | www.激情 | 脱了女方的内裤就开始做 | 色姑娘综合 | 超碰在线中文字幕 | 精品免费 | 一级片黄色 | 久久黄色录像 | 韩国三级hd中文字幕的背景音乐 | 黄色污污视频在线观看 | 免费一区二区在线观看 | 国产99久久精品一区二区永久免费 | 亚洲永久av | 午夜激情网址 | 国产精品自产拍高潮在线观看 | 嗯啊熟乳岳怀孕好深 | 一本久久综合 | 诱惑の诱惑筱田优在线播放 | 午夜在线视频 | 男男全程肉无删减电影 | 亚洲精品三区 | 啊灬岳灬啊灬快灬高潮了 | 少妇被挠肉丝脚心vk | 中文字幕在线播放视频 | 欧美做受69 | 亚洲激情久久 | 亚洲天堂av在线免费观看 | 亚洲videos | 五月激情视频 | 色偷偷网站 | 999热这里只有精品 av直接看 | 亚洲va天堂va欧美ⅴa在线 | 国产一区在线视频 | 日韩成人精品一区二区 | 美女爆吸乳羞羞免费网站妖精 | 亚洲熟妇色自偷自拍另类 | 亚洲第一页在线观看 | 日本久久免费 | 男女av在线| 久久综合九色综合欧美狠狠 | 成人吃奶视频 | 性日本xxx| 污网站在线看 | 国语播放老妇呻吟对白 | 国产成人91| 亚洲蜜桃精久久久久久久久久久久 | 欧洲三级电影 | 色偷偷综合 | 国产精品无码永久免费不卡 | 草莓视频在线观看污 | bl无遮挡高h动漫 | 日韩在线免费视频观看 | 亚洲国产日韩在线观看 | 在线爱情大片免费观看大全 | 成人一级黄色片 | 免费观看xxx在线观看下载 | 国产欧美a | 免费看一级片 | 制服丝袜在线一区 | 小视频黄色 | 国产精品a久久久久 | 日日插插 | 精品国产乱码久久久久久蜜柚 | 狂野欧美性猛交xxxx | 中文字幕第35页 | 美女性高潮视频 | 91亚洲精品久久久蜜桃网站 | 久久五月天婷婷 | 毛片毛片毛片毛片毛片 | 伊人欧美 | 谁有免费黄色网址 | 伊人影院综合 | 亚色成人| 国产精品久久久久久99 | 波多野结衣毛片 | 日日干夜夜草 | 在线播放黄色网址 | 欧美大片黄 | 中国黄色一级片 | 操女人逼逼视频 | 国产综合第一页 | 巨乳的诱惑 | 国产精品三级av | 天天操好逼| 久久久久无码精品国产 | 久久天堂影院 | 国模私拍xvideos私拍 | 国产传媒视频在线观看 | av高清免费 | 国产精品毛片一区二区三区 | 精品国产乱码久久久久久郑州公司 | 国产69精品久久久久毛片 | 激情图片在线视频 | 快色视频| 国产深夜福利 | 这里只有精品9 | 日日夜夜摸 | 亚洲成人精品一区二区三区 | 午夜宅男影院 | 性狂虐xxxxx变态胶衣胶奴视频 | 朝鲜黄色片 | 午夜性做爰电影 | 黄色三级在线视频 | 韩国伦理在线 | 在线观看理论片 | 国产一区二区精品丝袜 | 五月婷婷色 | 肉大捧一进一出免费视频 | 欧美熟妇另类久久久久久不卡 | 国产精品美女毛片真酒店 | 被夫上司蹂躏的七天七夜在线观看 | 国产精品毛片一区视频播 | 午夜影院黄色 | 老司机免费在线视频 | 欧美日韩一二三四 | 久久黄色大片 | 华人在线视频 | 在线观看中文字幕网站 | 女攻总攻大胸奶汁(高h) | 一区二区三区精品视频 | 女m被s玩胸虐乳哭着求饶 | 欧美精品在线一区 | 奇米四色7777 | 日韩精品一区二区三区免费视频 | 国产一级做a爰片在线看免费 | 天堂a√在线 | 禁漫天堂免费网站 | 成人av观看 | 天堂婷婷 | 人人干超碰 | 黄色片欧美 | 国产一级二级三级视频 | 亚洲123| 按摩害羞主妇中文字幕 | 永久91嫩草亚洲精品人人 | 91喷水 | 中文字幕网址 | 黄色精品网站 | 亚洲色图国产精品 | 欧美午夜精品久久久久久人妖 | 伊人久久久久久久久 | 永久看看免费大片 | 久久性色| 成人av日韩| 《给我播放》免费观看 | 羞羞漫画在线 | 91成年视频 | 女人裸体又黄 | 精品人伦一区二区三区 | 国产精品无码一区二区三区 | 写真福利片hd在线播放 | 日韩大片在线观看 | 日本白嫩的bbw | 在线观看免费 | 91tv国产成人福利 | 欧美黄色片 | h文网站 | 狠狠视频 | 国产精品夜夜夜爽张柏芝 | 人人妻人人澡人人爽人人欧美一区 | 51av在线| 亚洲综合婷婷 | 天堂a√在线 | 欧美精品中文字幕亚洲专区 | 国产精品亚洲一区 | 今天高清视频在线观看 | 成人在线观看网站 | 成年女人免费视频 | 一区二区三区国产在线观看 | www.狠狠| 少妇精品 | 婷婷成人在线 | 国产精品v亚洲精品v日韩精品 | 成人午夜又粗又硬又大 | 微拍福利一区二区 | 日本黄色免费观看 | 国内自拍视频在线观看 | 日韩精品一区二区三区四区五区 | 曰批女人视频在线观看 | 极品美女一区二区三区 | 九月丁香婷婷 | 偷啪自啪 | 国产精品一区在线观看 | 亚洲国产一 | 日韩欧美福利视频 | 国产调教在线观看 | 黄网站色视频 | 日韩另类小说 | 国产成人高清 | 婷婷丁香一区二区三区 | 亚洲欧美自偷自拍 | 欧美日韩电影一区 | 日韩精品一区二区三区免费视频 | 中国一级黄 | 中文字幕久久网 | 欧美第五页 | 亚洲成人黄色影院 | 亚洲天堂中文 | 亚洲免费在线播放 | 亚洲色图欧美在线 | 91动画| 91麻豆精品国产91久久久久久久久 | 超碰超碰超碰超碰 | 伊人久久艹 | 欧美精品videosbestsexhd4k | 欧美不卡一区二区三区 | 污网站免费观看 | 亚洲成年人专区 | 美女大黄动图 | 亚洲伊人色 | www狠狠| 午夜精产品一区二区在线观看的 | 久久天天躁狠狠躁夜夜爽蜜月 | 大伊人网 | 色黄网站在线观看 | 欧美黄色一区二区 | 天天操人人 | 国产美女一区二区三区 | 日本一本不卡 | 日韩中文字幕在线看 | 国产绿帽一区二区三区 | 福利视频在线看 | 一级毛片黄色 | 人人干超碰| av国产免费 | 精品人伦一区二区三区 | 国产91在线播放精品91 | 3级黄色片 | 性free公交车videos | 97成人资源 | 无人在线免费观看视频 | 丝袜ol美脚秘书在线播放 | 亚洲xx视频| 久久久久久影视 | 精品黑人一区二区三区在线观看 | 毛片毛片毛片毛片 | 日本精品人妻无码77777 | 成人看片网 | 国产男同gay男男麻豆 | www.自拍偷拍| 成年人在线观看免费视频 | 高清中文字幕在线a片 | 国产高清不卡视频 | 亲女禁h啪啪宫交 | 日本人妻一区| a级片黄色 | 亚洲成人精品一区二区 | 999视频| 同人动漫在线观看 | 在线观看超碰 | 日韩中文字幕高清 | 伊人久久中文 | 亚洲视频一区二区 | 做爰全过程叫床视频 | 林由奈在线观看 | 男女啪啪免费网站 | 欧美三级视频在线播放 | 成人教育av | 日韩欧美亚洲一区二区三区 | 亚洲另类av | 亚洲成年人专区 | 国产欧美久久久久久 | 91污免费| 日本高清不卡一区 | 一级片在线免费看 | 日韩av在线中文字幕 | 亚洲一区二区三区中文字幕 | 嘿咻免费视频 | 激情亚洲色图 | 他揉捏她两乳不停呻吟视频 | a级黄色在线观看 | 成年人av | 羞耻调教憋尿(高h,1v1) | 视频在线观看一区二区 | 国产美女免费视频 | 人妻丰满熟妇av无码久久洗澡 | 日韩一区免费 | 91亚洲精品国偷拍自产在线观看 | 国产三级在线免费观看 | 国产伦精品一区二区三区 | 女生被男生插 | 五月天婷婷网站 | 性欧美视频在线观看 | 狠狠干夜夜爱 | 婷婷激情小说 | 火影忍者小樱本子 | 成年人在线观看免费视频 | 黄视频免费在线观看 | 全是肉的高h文〈男男〉 | 17c在线观看视频 | 四虎av网站 | 99久久精品国产一区二区三区 | 妹妹av| 狠狠操免费视频 | 天天爱天天爽 | 五月婷婷丁香 | 俺也去五月婷婷 | 国产色视频 | 高压监狱法版免费观看全部 | 成人三级在线播放 | 亚洲人xxx| 小泽玛利亚一区二区 | 波多野结衣av在线观看 | 成年人在线观看免费视频 | 亚洲无人区码一码二码三码的含义 | 姐妹5免费观看完整 | 午夜在线视频 | 青青草草| 爱的精灵| 爱豆国产剧免费观看大全剧集 | 一级黄色片免费观看 | 日韩毛片在线免费观看 | 午夜视频免费 | 97色干| 雪中悍刀行2大牛影库 | 亚洲无人区码一码二码三码的含义 | 三级av在线 | www.日韩视频| www.成人在线观看 | 91福利影视 | 国产一级一片免费播放 | 口述我的初苞被强开 | 少妇献身老头系列 | 亚洲自拍中文字幕 | 中国挤奶哺乳午夜片 | 深夜福利你懂的 | 久久偷看各类女兵18女厕嘘嘘 | 欧美特级黄色录像 | 毛片网页 | 欧美极品视频 | 黄a在线 | 日韩综合一区 | 日韩色综合 | 狠狠婷婷 | 68日本xxxxxⅹxxx22| 午夜av在线播放 | 成人日韩精品 | 色综久久| 亚洲成人av一区二区三区 | 国产又粗又猛又黄视频 | 日韩一区二区视频在线 | 她享受粗啪滋嗯大爷轻点视频 | 欧美综合在线视频 | 亚洲精品国产精品乱码不卡 | 天堂a√在线| 色综合天天综合网天天狠天天 | 浮力影院国产第一页 | 老师露出强行让男生揉动漫 | 漂亮的岳hd中文字幕 | 国产精品午夜影院 | 一区二区不卡在线 | 国模无码视频一区 | 日韩高清精品免费观看 | 亚洲另类av | 日日骚av | 调教在线观看 | 成人h视频| -




 立即咨詢
立即咨詢 留言咨詢
留言咨詢



